过氧化物酶(peroxidase,POD)是植物体内一类活性较高的氧化还原酶,参与光合作用、呼吸作用以及抗病抗逆等多种生理活动[1,2,3]。POD作为一种生化标记,广泛应用在植物亲缘关系分析和某些表观性状的遗传分析[4,5,6]。王书玉等[4]对水稻亲本间苗期和孕穗期叶片POD进行分析,在子代中检测到新酶带,认为这可能是杂种优势形成的重要原因。陈立强等[5]对39份苜蓿材料进行POD同工酶分析,发现6条POD同工酶多态性较好,可以很好地用于分析苜蓿种间的亲缘关系。包海柱等[6]对大麦叶片保护酶模拟干旱胁迫下的发育遗传进行分析,发现在开花-灌浆阶段,POD加性效应和显性效应表现出基本等量强度的遗传效应,认为可以选择POD来分析F1开花-灌浆阶段的遗传效应。
1 材料和方法
1.1 材料
水稻试验材料,母本:“盐粳334-6”(用A表示);父本:“津星1号”(用B表示);子代:“新稻03518”,亲本杂交后代经6代自交选育获得稳定的株系(用C表示)。穗颈瘟抗性数据由江苏省农业科学院植物保护研究所提供,米质等级数据由农业农村部食品质量监督检验测试中心(武汉)提供。
1.2 试验方法
1.2.1 样品制备 试验材料统一于2017年5月1日育秧,6月3日移栽于土壤肥力一致的同一试验田(河南师范大学生物试验园地),田间管理按常规大田措施。待水稻生长至灌浆期取样,分别在灌浆前期、中期、后期分3次。每个样品设置3个重复,每个重复选5株取倒二叶片,用去离子水冲洗干净,吸干表面水分,去除叶脉后保留中间1cm左右叶片,在4℃环境条件下,5份剪碎混合称量,转移至预冷研钵中液氮充分研磨,然后加入4倍提取液(0.9% NaCl溶液)继续研磨至匀浆,转移至离心管冰浴浸取5min,4℃离心(10 000r/min)10min,取上清液分装到200μL离心管,-20℃保存备用。
1.2.2 复性电泳及成像分析 复性电泳技术(SDS-G-PAGE)参照徐存拴等[7]方法(略有改动),电泳采用10%分离胶和5%浓缩胶,样品制备液中加入活性样品缓冲液,混匀备用。各泳道上样量为30μL,浓缩胶电压≤80V,电流≤20mA,分离胶电压≤120V,电流≤20mA,置于4℃环境进行电泳。
电泳后胶板用洗涤液(TritonX-100 12mL,Tris-base 3.03g,加双蒸水500mL,调pH至7.0)漂洗30min,再用双蒸水洗涤3次,每次5min。染色参考姬生栋等[8]方法,待条带清晰后立即拍照。标准蛋白泳道(蛋白Marker分子量:245、180、135、100、75、63、48、35、25、20kD)洗涤前单独切下,固定后考马斯亮兰染色,然后脱色,拍照成像。
酶谱成像后采用Gel Pro软件(美国Media Cybernetics公司)分析标注各酶带分子量及每条酶带积分吸光度(integral optical density,IOD),各泳道内所有酶带IOD之和代表各泳道POD总酶活。
2 结果
2.1 亲本间性状比较
由表1可以看出,C的穗颈瘟病抗性与B相同,其余性状均介于A和B之间,其中株高、剑叶长、穗长和千粒重表现为偏A,单株分蘖数、穗总粒数、穗实粒数、米质和生育期表现为偏B。
表1 水稻C与亲本性状差异比较
Table 1
| 材料 Material | 株高(cm) Plant height | 剑叶长(cm) Length of flag leaf | 穗长(cm) Ear length | 单株有效分蘖/单株总分蘖 Effective tillers per plant/ Total tillers per plant | 穗总粒数 Grains per panicle | 穗实粒数 Solid grains per panicle | 千粒重(g) 1000-seed weight | 米质 Rice quality | 生育期(d) Growing period | 穗颈瘟 Rice blast disease |
|---|---|---|---|---|---|---|---|---|---|---|
| A | 105 | 36 | 23 | 17/20 | 175 | 163 | 26.11 | 等外 | 153 | 感 |
| B | 96 | 25 | 15 | 10/12 | 122 | 111 | 27.2 | 优2 | 165 | 中抗 |
| C | 98 | 26 | 19 | 13/15 | 125 | 113 | 26.27 | 优3 | 161 | 中抗 |
2.2 灌浆期POD酶谱
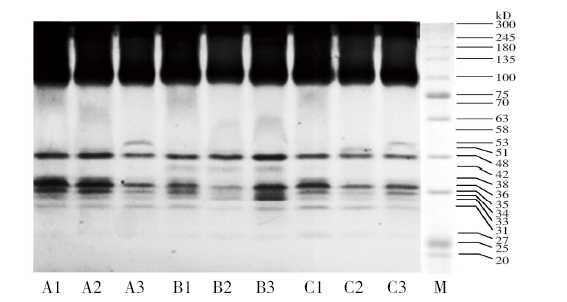
由图1中A1、B1、C1泳道可知,灌浆前期各泳道均检出300~100kD高酶活带区和75~70kD弱酶活带区,以及48、38、36、34、33、31和27kD等7条酶带。其中48kD酶活均较强,33、31和27kD酶活均较弱,而38、36和34kD酶活在各泳道差异明显,38kD酶活表现为:A1>C1>B1;36kD酶活表现为:A1>C1>B1;34kD酶活表现为:A1>B1>C1。B1检出一条42kD活性较弱酶带,在A1和C1未检出。
图1
图1
水稻子代和亲本灌浆期叶片POD酶谱
A,母本;B,父本;C,子代;编号1、2、3分别为灌浆前期、中期、后期;M为标准蛋白Marker。下同
Fig.1
The leaf POD zymogram of rice offspring and parents in grain filling stage
A, Female parent; B, Male parent; C, Offspring; The number 1, 2 and 3 were respectively in the early, middle and late stage of grain filling; M was the standard protein marker. The same below
灌浆中期POD酶谱见图1中A2、B2、C2泳道,除高酶活带区外,各泳道均检出48、36、33、31和27kD等5条酶带。其中48kD酶活均较强,33、31和27kD酶活均较弱,36kD酶活变化表现为A2>C2>B2。C2检出1条52kD新酶带,A2和B2均未检出;在A2中检出70~63kD弱酶活带区,B2中检出63~58kD弱酶活带区,这2个带区在C2中均未检出。A2和C2还检出34kD酶带,在B2中均未检出,34kD酶活表现为A2>C2;仅在A2中检出38kD酶带,B2和C2未检出。B2较A2和C2多检出42kD酶带。
灌浆后期POD酶谱见图1的A3、B3和C3泳道所示,除高酶活带区外,各泳道均检出48、36、34、33、31和27kD等6条酶带。其中48kD和36kD酶活均较强,31kD和27kD酶活均较弱,33kD酶活变化表现为B3>A3>C3。A3和C3检出1条53kD酶带,B3未检出;B3检出42kD酶带,A3和C3未检出。
2.3 POD总酶活变化
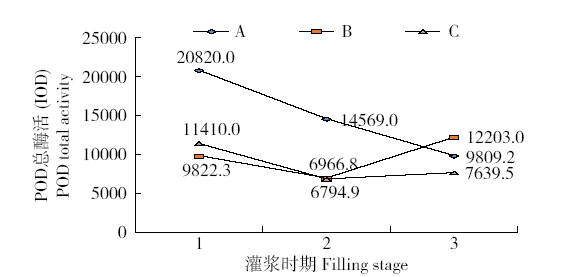
由图2可知,同一材料中不同时期POD总酶活变化表现为:A中各泳道总酶活表现为A1>A2>A3,B各泳道表现为B3>B1>B2,C各泳道表现为C1>C3>C2。同一时期亲本POD总酶活表现为:灌浆前期总酶活表现为A1>C1>B1,灌浆中期总酶活表现为A2>C2>B2,灌浆后期总酶活表现为B3>A3>C3。可以看出,A1、A2的POD总酶活较高,B3的POD总酶活较高,C在灌浆各时期POD总酶活变化规律为先降后升,与B较相似。各材料灌浆不同时期POD总酶活由高到低为:A1>A2>B3>C1>B1>A3>C3>B2>C2。
图2
图2
水稻子代和亲本灌浆期叶片POD总酶活
Fig.2
The leaf total POD activity of rice offspring and parents in grain filling stage
3 讨论
POD在遗传表达中具有相对稳定性,因此可根据水稻灌浆期叶片POD酶谱的动态变化来分析亲本间基因表达的差异。由研究结果可以看出,C“新稻03518”POD总酶活动态变化规律与B“津星1号”相似,表现为前期强、中期下降、后期酶活上升,B后期酶活明显高于A和C;A的POD总酶活变化近似直线下降,前期、中期明显高于C和B,后期则低于B而高于C。从遗传性状看,A生育期较C短6d,千粒重也稍低于C;C生育期较B短4d,千粒重较B低。可以看出,灌浆后期POD总酶活迅速下降的材料生育期短,灌浆后期POD总酶活上升的材料生育期也随之延长,且酶活越高生育期越长。POD能够清除活性氧,从而减少膜损伤,延缓叶片细胞衰老进程,进而延长植株的生育期。尹春佳等[9]对寒地超级稻叶片衰老过程中POD活性动态变化进行研究,发现生育后期超级稻POD活性高于常规品种,认为超级稻POD等保护酶活性高是延缓衰老、获得高产的生理基础。李江伟[10]对小麦灌浆后期叶片细胞衰老的POD活性变化进行研究,发现抗衰老株系总酶活强,易衰老株系总酶活低,认为小麦叶片灌浆后期细胞衰老与总酶活有关。杨晓娟等[11]对香稻不同生育时期活性氧的代谢差异进行研究,发现POD等酶活高的抗衰老能力强,认为POD酶活维持在高水平能延缓叶片生理衰老。以上研究结果表明,水稻灌浆期POD总酶活变化与代谢活动有关,一定范围内灌浆时期适当延长,能够使子粒灌浆更充分,提高粒重。
C在灌浆中期检出52kD新酶带,这种亲本未检出而C检出的新酶带被称为“杂交酶带”,新酶带的出现可能是C中基因表达受到共有基因互作,也可能是环境作用激活后代某些POD代谢途径。Schwartz[16]最早在研究玉米酯酶时发现杂交子代中出现亲本没有的新酶带,认为新酶带可能与杂种优势有关联。黄夕洋等[17]对三倍体罗汉果POD亲本间酶谱研究,发现子代中出现亲本没有的新酶带,认为出现新酶带的子代可能具有杂种优势。尹明智等[18]对油菜保持系和不育系不同时期的花蕾POD酶谱进行研究,发现不育系材料后期出现一条Rf=0.83的POD酶带,认为该酶带的出现和活性增强与花粉败育相关。灌浆中期叶片生理活动旺盛,POD参与到活性氧代谢、物质运输等多种代谢活动中,在C表型上未表现出与亲本差异明显的性状,这可能是由于检测的表观性状指标不够全面。至于新酶带是如何影响C的代谢活动还有待于进一步研究。
亲本间基因互作导致子代POD酶谱表达差异,这是育种希望得到的,进一步对于新酶带和差异酶谱与子代新性状关系的研究,发现亲本间的遗传关系,以及与水稻某个性状相关的酶带,为水稻生化标记辅助育种提供重要的理论依据。
参考文献
Latest development of antioxidant system and responses to stress in plant leaves
Genetic studies on mutant enzymes in maize:Synthesis of hybird enzymes by heterozygotes
DOI:10.1073/pnas.46.9.1210 URL [本文引用: 1]