作物杂志,2023, 第4期: 98–103 doi: 10.16035/j.issn.1001-7283.2023.04.015
紫花苜蓿胚性愈伤组织诱导及胚状体分化研究
王晓春1( ), 高婷1(
), 高婷1( ), 杨炜迪1, 王川1, 陈彩锦2
), 杨炜迪1, 王川1, 陈彩锦2
- 1宁夏农林科学院动物科学研究所,750000,宁夏银川
2宁夏农林科学院固原分院,756000,宁夏固原
Study on Embryogenic Callus Induction and Embryoid Differentiation of Alfalfa
Wang Xiaochun1( ), Gao Ting1(
), Gao Ting1( ), Yang Weidi1, Wang Chuan1, Chen Caijin2
), Yang Weidi1, Wang Chuan1, Chen Caijin2
- 1Institute of Animal Sciences, Ningxia Academy of Agriculture and Forestry Sciences, Yinchuan 750000, Ningxia, China
2Guyuan Branch of Ningxia Academy of Agriculture and Forestry Sciences,Guyuan 756000, Ningxia, China
摘要:
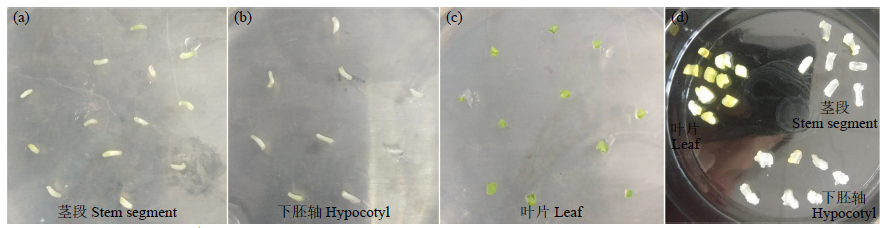
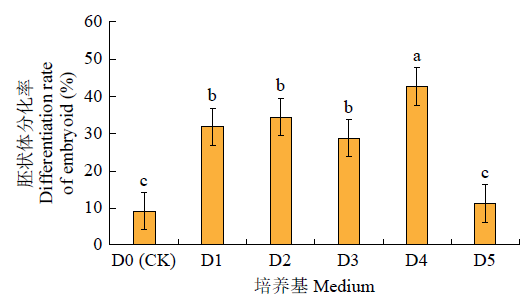
以苜蓿(固原紫花)下胚轴、茎段和叶片为外植体,开展了胚性愈伤组织的诱导及分化研究。结果表明,2,4-二氯苯氧乙酸(2,4-D)浓度为2和4mg/L时,愈伤组织诱导率为100.0%,浓度升为6和8mg/L时,诱导率逐渐降低,说明高浓度的2,4-D对苜蓿外植体愈伤组织诱导有抑制作用。MS培养基添加2,4-D(1.0、2.0、3.0、4.0mg/L),并配合0.5mg/L6-BA(6-苄基氨基嘌呤)或KT(激动素)后,3种外植体的诱导率均为100%,24d内能完全脱分化,且在质地和形态上无差别。转入分化培养基1/2MS后,所有配方都能分化出胚状体,2,4-D浓度2.0mg/L、KT浓度0.5mg/L组合的分化率最高(12.6%)。改进的分化培养基(1/2MS+0.4mg/LKT)分化率提高到42.7%。以诱导出的再生苗叶片和叶柄为外植体,发现体细胞胚胎诱导能力高度遗传,在添加2,4-D(1.0~8.0mg/L)组合0.5mg/L6-BA或KT的培养基内都能100%诱导出大量胚状体并发育为完整植株。由此可
见,通过再生植株可建立紫花苜蓿高频再生体系。
| [1] | 李阳, 亓雯雯, 李绍阳, 等. 苜蓿种子萌发和幼苗生长对温度、光照和埋深的响应. 生态学杂志, 2021, 40(2):332-339. |
| [2] | 金太成, 王悦, 吴艳菊, 等. 苜蓿次生胚遗传转化系统优化. 分子植物育种, 2019, 17(20):6685-6690. |
| [3] |
Von Arnold S, Sabala I, Bozhkov P, et al. Developmental pathways ofsomatic embryogenesis. Plant Cell, Tissue and Organ Culture, 2002, 69(3):233-249.
doi: 10.1023/A:1015673200621 |
| [4] | 李玉珠, 李巧璐, 范艳红, 等. 苜蓿下胚轴愈伤组织诱导和体细胞胚的发生与观察. 中国草地学报, 2014, 36(6):97-102. |
| [5] | 温之雨, 董福双, 张华宁, 等. 紫花苜蓿高频体胚发生及萌发成苗技术与转基因应用. 西北农业学报, 2017, 26(6):882-889. |
| [6] |
王晓春, 师尚礼, 梁慧敏, 等. 2,4-D和6-BA组合配比对金达苜蓿愈伤组织诱导与分化的影响. 草地学报, 2010, 18(2):219-222.
doi: 10.11733/j.issn.1007-0435.2010.02.014 |
| [7] | 张凌云, 师尚礼, 尹成学, 等. 俄罗斯杂花苜蓿再生体系的建立. 草业科学, 2013, 30(12):1995-2000. |
| [8] | 王成龙, 周美亮, 董雪妮, 等. 紫花苜蓿两种再生体系的优化及比较. 中国农业科技导报, 2015, 17(4):53-61. |
| [9] |
李娟, 张万军, 王涛. 黄花苜蓿高频植株再生体系建立的研究. 草地学报, 2014, 22(4):834-838.
doi: 10.11733/j.issn.1007-0435.2014.04.024 |
| [10] | 史毅, 马晖玲. 三个苜蓿品种植株高频再生体系的研究. 甘肃农业大学学报, 2014, 49(2):125-132. |
| [11] | 王静, 麻冬梅, 许兴, 等. 苜蓿高频再生体系的建立. 北方园艺, 2012(2):109-112. |
| [12] | 靳慧卿. 豆科牧草体细胞胚再生体系构建及其差异性比较研究. 呼和浩特:内蒙古农业大学, 2015. |
| [13] | 王英哲, 任伟, 徐博, 等. 根蘖型苜蓿高频再生体系的建立. 黑龙江畜牧兽医, 2017(7):174- 176,297-298. |
| [14] | 段亚楠, 卢福荣, 茹艺, 等. 紫花苜蓿组织培养高频再生体系的建立. 北方园艺, 2013(15):127-129. |
| [15] | 许来俊, 王成章, 严学兵, 等. 苜蓿植株再生体系研究进展. 草业科学, 2012, 29(8):1294-1301. |
| [16] |
赵金梅, 李芳, 周禾, 等. 紫花苜蓿组织培养体系的建立. 核农学报, 2010, 24(3):507-512.
doi: 10.11869/hnxb.2010.03.0507 |
| [17] |
Saunders J W, Bingham E T. Production of alfalfa plants from callus tissue. Crop Science, 1972, 12:804-808.
doi: 10.2135/cropsci1972.0011183X001200060026x |
| [18] | 李云玲, 苗锦山. 紫花苜蓿的组织培养与快繁技术研究. 安徽农学通报, 2013, 19(7):51-52. |
| [19] | 徐春波, 王勇, 赵海霞, 等. 紫花苜蓿高频组培再生体系影响因素研究. 草原与草坪, 2010, 30(4):55-63. |
| [20] |
Sairam R V, Franklin G, Hassel R, et al. A study on the effect of genotypes, plant growth regulators and sugars in promoting plant regeneration via organogenesis from soybean cotyledonary nodal callus. Plant Cell, Tissue and Organ Culture, 2003, 75(1):79-85.
doi: 10.1023/A:1024649122748 |
| [1] | 杨婉君, 潘香逾, 王秀华, 王璐, 赵岩. 119个苜蓿品种(系)产量和农艺性状的遗传多样性分析[J]. 作物杂志, 2020, (6): 17–22 |
| [2] | 李颜方,杜艳伟,张正,王高鸿,赵根有,赵晋锋,余爱丽. 农杆菌介导谷子成熟胚遗传转化体系的建立与优化[J]. 作物杂志, 2019, (3): 73–79 |
| [3] | 刘淑霞,魏国江,荆瑞勇,王丽艳,关向军,孙宇峰,王广达,韩如月,石杰,郭永霞. 接种中华根瘤菌SD101和避光对紫花苜蓿固氮和光合作用的影响[J]. 作物杂志, 2018, (5): 156–161 |
| [4] | 张微,王良群,刘勇,郝艳芳,杨伟,白鸿雁,武擘. 农杆菌介导高粱遗传转化的相关因素优化[J]. 作物杂志, 2018, (1): 56–61 |
| [5] | 梁晓,祁永,吝亚杰,石一均,曹卫东,刘忠宽,刘桂霞. 应用综合指标法和灰色关联度法对10个紫花苜蓿品种进行耐盐性评价[J]. 作物杂志, 2017, (4): 44–49 |
| [6] | 王敬东,马洪文,樊云芳,陈晓军. 盐稻8号遗传转化体系中不同抗生素种类与浓度的抑菌效果研究[J]. 作物杂志, 2016, (5): 61–66 |
| [7] | 崔科飞,代惠萍,朱佳妮,张阿芳. 硒胁迫对大叶紫花苜蓿生理特性的影响[J]. 作物杂志, 2016, (4): 133–136 |
| [8] | 张丽娟,陆建英,王昶,闵庚梅,杨晓明. 豌豆愈伤组织及不定芽诱导影响因素的研究[J]. 作物杂志, 2016, (3): 33–36 |
| [9] | 岑忠用,苏江,邓晰朝,谢彦军. 总酚含量及多酚氧化酶活性与岩黄连愈伤组织褐化的相关性研究[J]. 作物杂志, 2016, (1): 149–153 |
| [10] | 施伟梅, 王妙飞, 罗双慧, 等. 超声联合酶法提取紫花苜蓿总黄酮及其抗氧化性能研究[J]. 作物杂志, 2015, (6): 64–69 |
| [11] | 杨向黎, 韩凤英, 秦旭, 等. 紫花苜蓿几种主要害虫的化学防治试验[J]. 作物杂志, 2014, (2): 131–136 |
| [12] | 王萍, 徐娜, 王罡, 等. 高渗处理对不同基因型大豆未成熟子叶基因枪法转化效果的影响[J]. 作物杂志, 2013, (6): 26–30 |
| [13] | 袁文娅, 关淑艳, 马红丹, 等. 玉米自交系H99与齐319幼胚愈伤组织诱导条件的优化[J]. 作物杂志, 2013, (4): 48–51 |
| [14] | 陈萍, 沈振荣, 迟海峰, 等. 不同施肥处理对紫花苜蓿产量和株高的影响[J]. 作物杂志, 2013, (1): 91–94 |
| [15] | 王梓全, 姜丽丽, 曹士亮, 王石, 龚振平. 玉米叶基部愈伤组织诱导与植株再生[J]. 作物杂志, 2012, (6): 65–68 |
|
||