马铃薯StMYB3 基因的克隆、生物信息学及其表达分析
张宏宇 , 1 , 田再民 , 1 , 邱文萍 1 , 崔颖硕 1 , 桑乐飞 1 , 王雅宁 1 , 董书君 1 , 董莹莹 1 , 侯韶英 1 , 韩红艳 2 , 魏东 3
1 河北北方学院农林科技学院 , 075000 , 河北张家口
2 中化现代农业(内蒙古)有限公司 , 010000 , 内蒙古呼和浩特
3 河北北方学院/河北省农产品食品质量安全分析检测重点实验室 , 075000 , 河北张家口
Cloning, Bioinformatics, and Expression Analysis of StMYB3 Gene in Potato
Zhang Hongyu , 1 , Tian Zaimin , 1 , Qiu Wenping 1 , Cui Yingshuo 1 , Sang Lefei 1 , Wang Yaning 1 , Dong Shujun 1 , Dong Yingying 1 , Hou Shaoying 1 , Han Hongyan 2 , Wei Dong 3
1 College of Agriculture and Forestry Science and TechnologyHebei North University, Zhangjiakou 075000 , Hebei , China
2 Sinochem Modern Agriculture (Inner Mongolia) Co.Ltd., Hohhot 010000 , Inner Mongolia , China
3 Hebei North University / Hebei Key Laboratory of Agricultural Products and Food Safety Analysis and TestingZhangjiakou 075000 , Hebei , China
通讯作者: 田再民,主要从事马铃薯栽培与育种研究,E-mail:nkxtzm@163.com
收稿日期: 2024-11-19
修回日期: 2025-03-10
网络出版日期: 2025-05-22
基金资助:
河北北方学院博士基金 (BSJJ202428 )河北北方学院校级课题 (XJ2023019 )河北北方学院2024年大学生创新创业训练计划项目 (202410092013 )
Received: 2024-11-19
Revised: 2025-03-10
Online: 2025-05-22
作者简介 About authors
张宏宇,主要从事马铃薯栽培与育种研究,E-mail:2458479956@qq.com
摘要
马铃薯转录因子对花青素的影响主要体现在对马铃薯花青素合成途径相关转录因子的调控作用上。通过RT-PCR从马铃薯品种夏坡蒂(薯肉为白色)、万紫千红(薯肉为浅紫色)和2013-89-61(薯肉为深紫色)中克隆出马铃薯StMYB3 基因,对其进行生物信息学分析和差异表达分析。结果表明,马铃薯StMYB3 基因目的片段长度为710 bp,编码的蛋白分子质量20.71 kDa,等电点9.14,属于亲水性蛋白。马铃薯StMYB3 基因含有R2R3-MYB结构域和bHLH转录因子,不含跨膜结构域,系统进化分析表明马铃薯StMYB3 基因与辣椒ScMYB 序列相似度最高。经半定量PCR发现,马铃薯StMYB3 基因在不同部位表达量为嫩叶>老叶>茎>块茎>根,2013-89-61品种在各部位均属于高表达。
关键词:
马铃薯 花青素 StMYB3 生物信息学 表达分析
Abstract
The influence of potato transcription factors on anthocyanin accumulation is primarily reflected in their regulation of genes involved in the anthocyanin biosynthetic pathway. In this study, the StMYB3 gene was cloned by RT-PCR from three potato cultivars: Shepody (white flesh), Wanziqianhong (light purple flesh), and 2013-89-61 (dark purple flesh). Bioinformatics characterization and differential expression analysis were performed. The results showed that the target fragment of StMYB3 genes was 710 bp in length, encoding a protein with a molecular weight of 20.71 kDa and an isoelectric point of 9.14, which was identified as a hydrophilic protein. StMYB3 genes contains R2R3-MYB domain and bHLH interaction motif but lacks a transmembrane domain. Phylogenetic analysis revealed that StMYB3 genes shares the highest sequence similarity with the ScMYB gene from pepper. Semi-quantitative PCR results showed that the expression level of potato StMYB3 gene in different tissues is: tender leaf > old leaf > stem > tuber > root, and the cultivar 2013-89-61 exhibited consistently high expression across all tissues.
Keywords:
Potato Anthocyanins StMYB3 Bioinformatics Expression analysis
本文引用格式
张宏宇, 田再民, 邱文萍, 崔颖硕, 桑乐飞, 王雅宁, 董书君, 董莹莹, 侯韶英, 韩红艳, 魏东. 马铃薯StMYB3 基因的克隆、生物信息学及其表达分析 . 作物杂志 , 2026, 42(2): 68-73 doi:10.16035/j.issn.1001-7283.2026.02.008
Zhang Hongyu, Tian Zaimin, Qiu Wenping, Cui Yingshuo, Sang Lefei, Wang Yaning, Dong Shujun, Dong Yingying, Hou Shaoying, Han Hongyan, Wei Dong. Cloning, Bioinformatics, and Expression Analysis of StMYB3 Gene in Potato . Crops
我国马铃薯产业发展迅猛,随着生活水平的提升,人们对马铃薯食品的需求也逐渐从满足温饱向追求更高的营养保健价值转变[1 ] 。花青素具有抗氧化、保护视力、降低心血管疾病风险以及提高人体免疫力及抗炎等功能,因而富含高花青素含量的彩色马铃薯成为马铃薯产业的研究热点[2 -3 ] 。植物中的花青素是一种天然水溶性色素,能使植物呈现出各种颜色[4 ] 。马铃薯的薯肉通常呈白色或黄色,此外,紫色和红色等彩色马铃薯中的花青素含量相对较高。植物中花青素的合成代谢受到转录因子的调控,目前,已鉴定出3类参与花青素代谢合成的转录因子,分别为MYB家族成员、BHLH蛋白和WD40因子,其中R2R3-MYB为最主要的转录调控因子[5 ] 。
MYB转录因子是植物中最大的一类转录因子家族,其重要的功能之一是调控花青素的合成[6 ] 。MYB转录因子在结构上有一段位于N端的保守DNA结合区(MYB结构域),主要负责对靶基因上游启动子区域顺式作用元件的识别与结合[7 ] 。MYB结构域通常是由不完全重复的氨基酸序列组成,重复序列R可分为R1、R2和R3,结构域之间的组合又可形成4种类型的MYB蛋白,分别为单-MYB结构域(R1/2、R3)蛋白、2R(R2R3)蛋白、3R(R1R2R3)蛋白和4R(R1R2R2R1/2)蛋白[8 ] ,广泛分布于植物中并发挥着重要的生物学功能,包括植物的生长发育、次级代谢调控和胁迫应答等。MYB转录因子还可以正向或负向调节花青素的生物合成[9 ] 。史程程等[10 ] 采用RT-PCR方法在葡萄风信子中克隆获得1个MaMYB114 基因,对其进行生物信息学分析和异源转化烟草功能验证,表明其正向调控花青素合成。周薇[11 ] 从中华红叶杨中分离了花青素合成相关转录因子MYB118L 基因并对其蛋白序列特征、亚细胞定位、功能与作用机制进行探究,初步揭示了MYB118L 基因调控花青素合成过程的分子机制。鲁亚楠[12 ] 通过转录组和RT-PCR分析发现文冠果中的XsMYB113-1 、XsMYB113-2 、XsMYB113-3 和XsMYB113-4 基因均能正向调控花青素的合成。通过多个试验,不同植物中的MYB转录因子均被证实能够调控花青素合成,揭示了MYB转录因子在花青素生物合成途径中的关键作用。
本试验从马铃薯品种夏坡蒂(Shepody)、万紫千红(WZQH)以及2013-89-61中克隆获得马铃薯StMYB3 基因,对其进行生物信息学分析,并利用RT-PCR技术分析马铃薯StMYB3 基因在马铃薯不同品种和不同组织中的表达,为进一步深入研究马铃薯StMYB3 转录因子功能提供理论依据。
1 材料与方法
1.1 试验材料
供试马铃薯品种为夏坡蒂(薯肉为白色)、万紫千红(薯肉为浅紫色)和2013-89-61(薯肉为深紫色)。
1.2 试验地概况
试验材料种植于河北省张北县河北北方学院试验基地。田间播种采用随机区组设计,每个品种种植5行,3次重复,行长6 m,行距70 cm,种植密度52 500株/hm2 。采用正常田间管理,在盛花期取叶、茎和根的样本,在成熟期取块茎样本,在液氮中速冻后存放于-80 ℃。针对每个样本,于每次重复中选取3株并进行混合。
1.3 测定项目与方法
1.3.1 总RNA的提取
使用Trizol植物总RNA提取试剂盒(Plant RNApure Kit)提取RNA,用1%琼脂糖凝胶电泳检测RNA。
1.3.2 cDNA的合成
以马铃薯提取的总RNA为模板,在PCR管中加入试剂2 μL 5× g DNA Eraser Buffer、1 μL gDNA Eraser、5 μL总RNA,用Rnase-free ddH2 O,定容至10 μL。42 ℃ 2 min(或者室温5 min)去除基因组DNA污染。再加入1 μL Primescript PT Enzyme Mix I、1 μL RT Primer Mix、4 μL 5×Primescript Buffer 2和4 μL RNase-free ddH2 O。在PCR仪上进行反转录,反应程序为37 ℃ 15 min,85 ℃ 5 s。
1.3.3 基因克隆
利用Primer 5.0软件设计引物。StMYB3-F 的引物序列(5′-3′)为CTACTTCAC ACAGTCTGATCCATCC;StMYB3-R 的引物序列(5′-3′)为AGATCGAGTTCATAACGATGATGTC。取0.2 mL离心管,加入13 μL ddH2 O、2.5 μL StMYB3 -F(10 μmol/L)、2.5 μL StMYB3 -R(10 μmol/L),2 μL cDNA及20 μL 2×Vazyme Lamp Master Mix。PCR扩增程序:94 ℃预变性3 min;94 ℃变性40 s,60 ℃退火40 s,72 ℃延伸40 s,循环35次;72 ℃修复延伸10 min。
1.3.4 马铃薯StMYB3 基因扩增产物的检测
(1)制备1%琼脂糖凝胶,加入5 μL核酸染料,混匀后倒入凝胶模具中,静置20 min,凝胶凝固后放入电泳槽,并加入电泳缓冲液。(2)加样,10 μL PCR产物样品,3 μL D2000 DNA Marker。(3)连接电泳,电压150 V,电流110 mA,电泳20 min,取出凝胶放入凝胶成像仪中成像。
1.4 生物信息学分析
利用NCBI完成马铃薯StMYB3 基因的ORF查找和氨基酸序列的推导;用ProtParam-EXPASY(http://www.expasy.org/tools/protparam.html )完成蛋白分子量和理论等电点的分析;用DNAMAN完成多序列氨基酸的比对;用MEGA构建系统进化树;用Expasy(http://au.Expasy.ch/tools/protscale.html )工具完成蛋白疏水性分析;用EXPASY(http://www.expasy.org/ )构建蛋白质的三级结构;用SOPMA(http:pbil.ibcp.fr/)构建蛋白质的二级结构;用TMHMM SERVER(www.cbs.dtu.dk/services/)完成蛋白质的跨膜区预测。
1.5 数据处理
用SPSS16.0软件进行方差分析,使用新复极差法进行显著性比较。
2 结果与分析
2.1 马铃薯StMYB3 基因的克隆
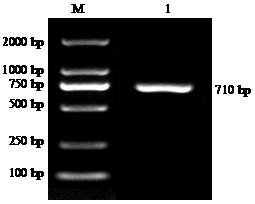
电泳结果(图1 )显示,在710 bp处有马铃薯StMYB3 基因的清晰条带。
图1
图1
马铃薯StMYB3 基因PCR产物的电泳结果
M:D2000 DNA分子量标准;1:StMYB3 基因片段。
Fig.1
Electrophoretic results of PCR products of potato StMYB3 gene
M: D2000 DNA Marker; 1: StMYB3 gene fragment.
2.2 马铃薯StMYB3蛋白序列比对和进化树的构建
在NCBI中利用BLAST查找其他物种MYB3 基因编码的同源蛋白序列进行比对,马铃薯StMYB3蛋白序列与辣椒(Solanum chilense )(TMW93937.1)、龙葵(Solanum penneli )(XP_015075126.1)、番茄(Solanum lycopersicum )(XP_004239398.1)、烟草(Nicotiana tabacum )(XP_016502778.1)和枸杞(Lycium barbarum )(XP_060214648.1)的序列一致性都在100%;与曼陀罗(Datura stramonium )(MCD7451847.1)的序列一致性为89%;与睡莲(Nymphaea thermarum )(KAF3792456.1)、石榴(Punica granatum )(XP_031403013.1)、栗子(Castanea mollissima )(KAF3943083.1)、紫荆花(Bauhinia variegata )(KAI4313806.1)和葡萄(Vitis vinifera )(RVW17057.1)的序列一致性均为99%,整体序列一致性范围为89%~100%,表明该MYB蛋白在不同物种间具有高度保守性。通过DNAMAN进行同源蛋白序列比对,如图2 所示,马铃薯StMYB3蛋白序列中存在R2R3-MYB结构域,其中包含bHLH转录因子。
图2
图2
马铃薯StMYB3蛋白的多序列对比
结构域为R2R3-MYB结构域和bHLH转录因子。
Fig.2
Multiple sequence alignment of the StMYB3 protein in potato
The domain is the R2R3-MYB domain and the bHLH transcription factor.
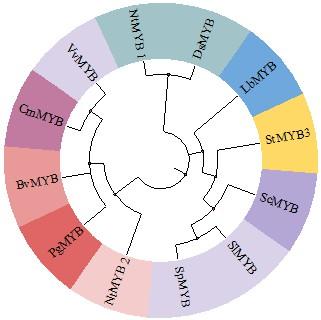
通过MEGA构建系统进化树,如图3 所示,马铃薯StMYB3蛋白与辣椒ScMYB蛋白在同一支上,同源关系最近,而茄科龙葵SpMYB和番茄SlMYB在另一个分支。
图3
图3
马铃薯StMYB3蛋白与其他物种MYB蛋白的系统进化树
Fig.3
Phylogenetic tree of potato StMYB3 protein and MYB proteins of other species
2.3 马铃薯StMYB3蛋白分子量和理论等电点分析
通过ProtParam软件在线预测分析:马铃薯StMYB3 基因编码的蛋白分子式为C904 H1441 N273 O266 S10 ,分子质量为20710.65 Da,理论等电点为9.14,带负电荷的氨基酸残基(Asp+ Glu)为23个,带正电荷的氨基酸残基(Arg+Lys)30个;不稳定系数为59.62,均为不稳定蛋白(不稳定系数<40为稳定蛋白),理论推导半衰期大约为30 h;脂肪系数平均为80.06,总平均亲水性为-0.822。
2.4 马铃薯StMYB3蛋白亲水性和疏水性分析
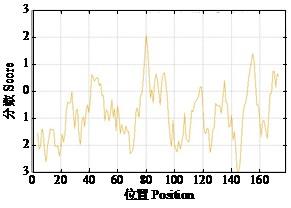
利用Expasy工具中的ProtScale软件在线分析。马铃薯StMYB3蛋白的亲水性分析见图4 。结果表明,马铃薯StMYB3 基因所编码的蛋白亲水性氨基酸均匀分布在整个肽链中,且多于疏水性氨基酸,为亲水蛋白。
图4
图4
马铃薯StMYB3蛋白的疏水性分析
Fig.4
Hydrophobicity analysis of potato StMYB3 protein
2.5 马铃薯StMYB3蛋白质二级结构和三级结构的预测
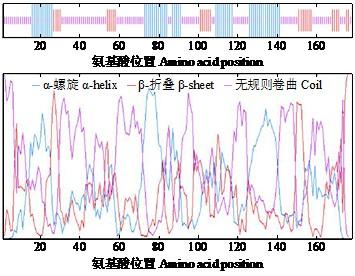
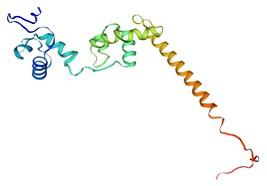
对SOPMA进行蛋白质二级结构的预测,如图5 所示,马铃薯StMYB3蛋白质二级结构以无规则卷曲为主,其次为α-螺旋,β-折叠最少。通过在线网址进行蛋白质三级结构的预测,获得马铃薯StMYB3蛋白质三级结构图(图6 ),形状呈倒“L”型。
图5
图5
马铃薯StMYB3蛋白质二级结构预测
Fig.5
Secondary structure prediction of potato StMYB3 protein
图6
图6
马铃薯StMYB3蛋白质三级结构预测
Fig.6
Tertiary structure prediction of potato StMYB3 protein
2.6 马铃薯StMYB3蛋白序列跨膜区预测
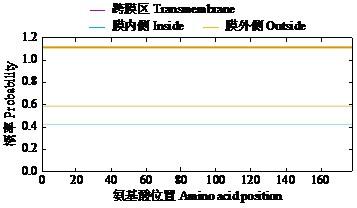
利用TMHMM工具对马铃薯StMYB3蛋白进行跨膜结构域预测,结果显示该蛋白序列中无跨膜螺旋结构区,跨膜区概率始终为0,胞内区与胞质区概率分布稳定,表明StMYB3属于非跨膜蛋白,符合转录因子的典型定位特征(图7 )。
图7
图7
马铃薯StMYB3蛋白跨膜结构域分析
Fig.7
Transmembrane domain analysis of potato StMYB3 protein
2.7 马铃薯StMYB3 基因在不同组织部位的表达模式分析
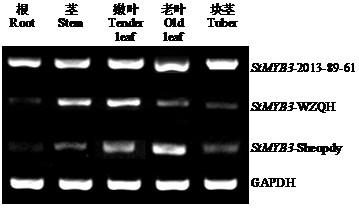
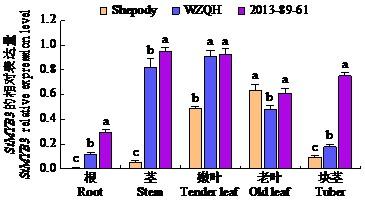
通过半定量RT-PCR克隆目的基因和内参基因GAPDH (图8 ),利用Quantity-One软件分析马铃薯StMYB3 基因在不同品种和不同部位的表达(图9 )。在根、茎、嫩叶和块茎中3个品种表达量均为2013-89-61>万紫千红>夏坡蒂;在老叶中表达量为夏坡蒂>2013-89-61>万紫千红。老叶中夏坡蒂的表达量最高,嫩叶中万紫千红表达量最高,茎中2013-89-61表达量最高,3个品种均在根中表达量最低。在不同部位中,表达量为嫩叶>老叶>茎>块茎>根,该基因在嫩叶中表达最高,3个马铃薯品种在根、茎和块茎中表达具有显著差异。
图8
图8
马铃薯StMYB3 基因在3个品种不同组织中的表达
Fig.8
Expression of potato StMYB3 gene in different tissues of three potato varieties
图9
图9
马铃薯StMYB3 基因的相对表达量
不同小写字母表示P < 0.05水平的差异显著性。
Fig.9
The relative expression level of StMYB3 in potato
Different lowercase letters indicate significant differences at P < 0.05 level.
3 讨论
在花青素合成调控中,MYB与bHLH、WD40单独作用,或者三者形成MBW复合体调控花青素的合成[13 ] 。MYB与MYC转录因子bHLH具备结合活性,二者共同调控花青素合成晚期基因的表达[14 ] 。本研究在马铃薯StMYB3蛋白序列中,发现了R2R3-MYB结构域的存在,这一结构域中还包含了与bHLH转录因子的相互作用。通过对不同品种和不同部位马铃薯StMYB3 基因的表达分析,发现该基因在嫩叶中表达最高,而且马铃薯StMYB3 基因在2013-89-61(薯肉深紫色)的根、茎、嫩叶和块茎中表达量均为最高,因此马铃薯StMYB3 基因可能参与马铃薯花青素合成的代谢路径。这与前人在研究马铃薯MYB转录因子的功能结果相近,例如,Lu等[15 ] 和Zhang等[16 ] 发现在马铃薯块茎中克隆到的R2R3-MYB转录因子中有共表达因子StbHLH1,在细胞核中表达且增强了MYB对花青素合成的调节作用。Jung等[17 ] 和许芸梅等[18 ] 对马铃薯红色薯肉基因进行了定位和筛选,发现其候选基因为R2R3-MYB转录因子,与控制薯皮花青素积累的StAN2 (D/I)相同。Liu等[19 ] 等研究了3个与R2R3- MYB转录因子(StAN1、StMYBA1和StMYB113)相关的功能,发现StMYBA1和StMYB113可以激活花青素的积累,且均具有部分R2R3结构域。而StbHLH1和StJAF13是花青素生物合成的关键共调节因子,StAN1、StMYBA1和StMYB113即使在没有色素积累的情况下也能表达。Rommens等[20 ] 发现MYB转录因子StMtf1 转基因植株基因激活了苯丙烷类生物合成路径,与对照相比,转基因块茎中的咖啡酰奎宁酸含量增加了4倍,包括绿原酸(CGA),同时也积累了黄酮醇和花青素。上述研究均表明MYB转录因子是花青素合成调控中的核心元件,其与其他转录因子的相互作用构成了调控花青素合成的关键机制。在马铃薯中,MYB转录因子不仅在马铃薯的花青素合成中发挥着关键作用,其还在不同组织(例如薯肉和薯皮)中具有调控作用。因此,马铃薯StMYB3 基因的更多功能需要亚细胞定位和转基因操作等进行进一步验证。
4 结论
从马铃薯品种夏坡蒂、万紫千红和2013-89-61中克隆获得StMYB3 基因,StMYB3 基因编码的蛋白属亲水蛋白,不含跨膜结构域,其蛋白质二级和三级结构高度相似,且马铃薯StMYB3 基因具有MYB家族的典型特征。RT-PCR结果表明2013- 89-61表达量在不同组织部位均高于夏坡蒂和万紫千红,且在块茎中表达差异更显著,3个马铃薯品种在根、茎、块茎中表达具有显著差异,证明马铃薯StMYB3 基因可以调控花青素的形成。
参考文献
View Option
[1]
郝智勇 , 杨广东 , 邱广伟 , 等 . 马铃薯高类胡萝卜素资源材料筛选
作物杂志 , 2019 (2 ):71 -77 .
[本文引用: 1]
[2]
李景伟 . 彩色马铃薯高密度SNP遗传连锁图谱构建及花青素含量等重要性状的QTL定位 . 呼和浩特 : 内蒙古农业大学 , 2022 .
[本文引用: 1]
[3]
史瑞翔 , 李博雯 , 孙圣卿 , 等 . 彩色马铃薯产量和品质性状评价
中国马铃薯 , 2022 , 36 (6 ):481 -488 .
[本文引用: 1]
[4]
聂利珍 , 李晓东 , 谢锐 , 等 . 彩色马铃薯查尔酮合酶基因的克隆及生物信息学分析
分子植物育种 , 2022 , 20 (23 ):7679 -7686 .
[本文引用: 1]
[5]
刘玉汇 . MYB和BHLH转录因子对马铃薯块茎花色素苷生物合成的调控机理研究 . 兰州 : 甘肃农业大学 , 2016 .
[本文引用: 1]
[6]
孙保娟 , 李涛 , 游倩 , 等 . 茄科植物花青素合成相关的MYB转录因子研究进展
中国农学通报 , 2023 , 39 (36 ):102 -111 .
DOI:10.11924/j.issn.1000-6850.casb2023-0035
[本文引用: 1]
MYB转录因子是植物中最大的一类转录因子家族,其重要的功能之一是调控花青素的合成。为了全面了解MYB转录因子对茄科植物花青素合成的调控作用,本研究从基因分离克隆、时空表达、调控方式等方面归纳了矮牵牛、马铃薯、番茄、辣椒、茄子、烟草、枸杞等7种茄科植物与花青素合成相关的MYB转录因子的研究进展。通过对已报道的茄科植物花青素代谢途径相关的MYB转录因子基因进行系统发育分析,发现不同茄科植物上激活型和抑制型MYB转录因子按功能聚类;调控果实花青素合成的关键MYB转录因子基因SlANT1、SmMYB1、StAN1、StAN2优先聚为一类,再与StMYBA1、SlAN2和LrAN2-like聚为一类;SlAN2-like、SmMYB2、StMYB113、LrMYB1以及CaMYB聚为一类;番茄的SlAN2和SlMYB75为不同命名的相同基因;茄子的SmMYB1、SmMYB6和SmMYB113为不同命名的同一MYB转录因子基因。本文指出了有关花青素合成的MYB转录因子基因在茄科蔬菜上进一步的研究方向,为茄科蔬菜花青素合成组织特异性调控机制解析以及通过基因调控和基因工程改良果色等方面的研究提供参考。
[7]
Thompson M A Ramsay R G MYB: an old oncoprotein with new roles
BioEssays , 1995 , 17 (4 ):341 -350 .
PMID:7741726
[本文引用: 1]
Over the last decade, the c-myb gene and its protein product, Myb, have undergone extensive examination and manipulation in hemopoietic tissues. Although it is rarely disputed that, as a transcription factor, Myb regulates cell cycling, proliferation and differentiation, identification of genes directly controlled by Myb has been surprisingly difficult. More recently, genes with promoter regions that contain Myb recognition sequences have been identified, but a direct proliferative response to Myb via these 'target genes' has yet to be demonstrated. Mutagenesis studies have defined domains of the protein which influence its transcriptional activity and transforming potential; however how the molecule interacts with itself and with other cellular factors is only beginning to be understood. A broader examination of c-myb expression in normal and malignant tissues suggests an analogous role for Myb in proliferation, differentiation and transformation of non-hemopoietic tissues.
[9]
余斌 , 杨宏羽 , 王丽 , 等 . 引进马铃薯种质资源在干旱半干旱区的表型性状遗传多样性分析及综合评价
作物学报 , 2018 , 44 (1 ):63 -74 .
[本文引用: 1]
[10]
史程程 , 陈鹏 , 焦清正 , 等 . 葡萄风信子Ma MYB114 基因的克隆及功能研究
西北植物学报 , 2023 , 43 (12 ):2039 -2048 .
[本文引用: 1]
[11]
周薇 . 杨树MYB118L 基因调控花青素合成机制研究 . 宜昌 : 三峡大学 , 2023 .
[本文引用: 1]
[12]
鲁亚楠 . 文冠果XsMYB113 调控花色渐变的分子机制 . 哈尔滨 : 东北林业大学 , 2022 .
[本文引用: 1]
[13]
王卫强 , 钟巍然 , 鞠远金 , 等 . 不同栽培条件对马铃薯紫云1号花青素含量影响的研究
西南农业学报 , 2010 , 23 (5 ):1439 -1442 .
[本文引用: 1]
[14]
Chiu L W Li L Characterization of the regulatory network of BoMYB2 in controlling anthocyanin biosynthesis in purple cauliflower
Planta , 2012 , 236 (4 ):1153 -1164 .
DOI:10.1007/s00425-012-1665-3
PMID:22644767
[本文引用: 1]
Purple cauliflower (Brassica oleracea L. var. botrytis) Graffiti represents a unique mutant in conferring ectopic anthocyanin biosynthesis, which is caused by the tissue-specific activation of BoMYB2, an ortholog of Arabidopsis PAP2 or MYB113. To gain a better understanding of the regulatory network of anthocyanin biosynthesis, we investigated the interaction among cauliflower MYB-bHLH-WD40 network proteins and examined the interplay of BoMYB2 with various bHLH transcription factors in planta. Yeast two-hybrid studies revealed that cauliflower BoMYBs along with the other regulators formed the MYB-bHLH-WD40 complexes and BobHLH1 acted as a bridge between BoMYB and BoWD40-1 proteins. Different BoMYBs exhibited different binding activity to BobHLH1. Examination of the BoMYB2 transgenic lines in Arabidopsis bHLH mutant backgrounds demonstrated that TT8, EGL3, and GL3 were all involved in the BoMYB2-mediated anthocyanin biosynthesis. Expression of BoMYB2 in Arabidopsis caused up-regulation of AtTT8 and AtEGL3 as well as a subset of anthocyanin structural genes encoding flavonoid 3'-hydroxylase, dihydroflavonol 4-reductase, and leucoanthocyanidin dioxygenase. Taken together, our results show that MYB-bHLH-WD40 network transcription factors regulated the bHLH gene expression, which may represent a critical feature in the control of anthocyanin biosynthesis. BoMYB2 together with various BobHLHs specifically regulated the late anthocyanin biosynthetic pathway genes for anthocyanin biosynthesis. Our findings provide additional information for the complicated regulatory network of anthocyanin biosynthesis and the transcriptional regulation of transcription factors in vegetable crops.
[15]
Lu Q N Yang Q cDNA cloning and expression of anthocyanin biosynthetic genes in wild potato (Solanum pinnatisectum )
African Journal of Biotechnology , 2006 , 5 (10 ):811 -818 .
[本文引用: 1]
[16]
Zhang Y F Jung C S De J W S Genetic analysis of pigmented tuber flesh in potato
Theoretical and Applied Genetics , 2009 , 119 (1 ):143 -150 .
DOI:10.1007/s00122-009-1024-3
PMID:19363602
[本文引用: 1]
Interest in anthocyanin-pigmented potato tuber flesh is increasing. To genetically map and characterize loci that influence this trait, diploid potato clone 10618-01, which has partially pigmented flesh, was crossed with diploid 320-02, which has white flesh. Almost all progeny exhibited purple coloration in the flesh, with some clones having only a small percentage of tissue pigmented, other clones having most tissue pigmented, and the majority of clones showing intermediate color phenotypes. The two parents and 228 progeny were genotyped with 493 AFLP, 8 CAPS, and 13 SSR markers. QTLs influencing extent of flesh pigmentation were detected on chromosomes 5, 8, and 9. The potato homolog of Petunia an1, a basic helix-loop-helix (bHLH) transcriptional regulator of anthocyanin biosynthesis, was found to co-localize with the QTL on chromosome 9. A CAPS marker based on this gene was used to evaluate a collection of 21 tetraploid potato clones with highly or fully pigmented red or purple flesh, as well as 53 cultivars with white or yellow flesh. All 21 pigmented-flesh clones shared a marker allele that was present in only 21 of the 53 white and yellow clones, suggesting that a common bHLH allele contributes toward, although it is clearly not sufficient for, highly or fully pigmented tuber flesh in cultivated potato.
[17]
Jung C S Griffiths H M Jong D M D et al . The potato developer(D) locus encodes an R2R3 MYB transcription factor that regulates expression of multiple anthocyanin structural genes in tuber skin
Theoretical and Applied Genetics , 2009 , 120 (1 ):45 -57 .
DOI:10.1007/s00122-009-1158-3
URL
[本文引用: 1]
[18]
许芸梅 , 李玉梅 , 贾玉鑫 , 等 . 马铃薯红色薯肉调控基因的精细定位与候选基因分析
中国农业科学 , 2019 , 52 (5 ):2678 -2685 .
[本文引用: 1]
[19]
Liu Y H Wang K L Espley R V et al . Functional diversification of the potato R2R3 MYB anthocyanin activators AN1, MYBA1, and MYB113 and their interaction with basic helixloop-helix cofactors
Journal of Experimental Botany , 2016 , 67 (8 ):2159 -2176 .
DOI:10.1093/jxb/erw014
URL
[本文引用: 1]
[20]
Rommens C M Richael C M Yan H et al . Engineered native pathways for high kaempferol and caffeoylquinate production in potato
Plant Biotechnology Journal , 2010 , 6 (9 ):870 -886 .
DOI:10.1111/pbi.2008.6.issue-9
URL
[本文引用: 1]
马铃薯高类胡萝卜素资源材料筛选
1
2019
... 我国马铃薯产业发展迅猛,随着生活水平的提升,人们对马铃薯食品的需求也逐渐从满足温饱向追求更高的营养保健价值转变[1 ] .花青素具有抗氧化、保护视力、降低心血管疾病风险以及提高人体免疫力及抗炎等功能,因而富含高花青素含量的彩色马铃薯成为马铃薯产业的研究热点[2 -3 ] .植物中的花青素是一种天然水溶性色素,能使植物呈现出各种颜色[4 ] .马铃薯的薯肉通常呈白色或黄色,此外,紫色和红色等彩色马铃薯中的花青素含量相对较高.植物中花青素的合成代谢受到转录因子的调控,目前,已鉴定出3类参与花青素代谢合成的转录因子,分别为MYB家族成员、BHLH蛋白和WD40因子,其中R2R3-MYB为最主要的转录调控因子[5 ] . ...
1
2022
... 我国马铃薯产业发展迅猛,随着生活水平的提升,人们对马铃薯食品的需求也逐渐从满足温饱向追求更高的营养保健价值转变[1 ] .花青素具有抗氧化、保护视力、降低心血管疾病风险以及提高人体免疫力及抗炎等功能,因而富含高花青素含量的彩色马铃薯成为马铃薯产业的研究热点[2 -3 ] .植物中的花青素是一种天然水溶性色素,能使植物呈现出各种颜色[4 ] .马铃薯的薯肉通常呈白色或黄色,此外,紫色和红色等彩色马铃薯中的花青素含量相对较高.植物中花青素的合成代谢受到转录因子的调控,目前,已鉴定出3类参与花青素代谢合成的转录因子,分别为MYB家族成员、BHLH蛋白和WD40因子,其中R2R3-MYB为最主要的转录调控因子[5 ] . ...
彩色马铃薯产量和品质性状评价
1
2022
... 我国马铃薯产业发展迅猛,随着生活水平的提升,人们对马铃薯食品的需求也逐渐从满足温饱向追求更高的营养保健价值转变[1 ] .花青素具有抗氧化、保护视力、降低心血管疾病风险以及提高人体免疫力及抗炎等功能,因而富含高花青素含量的彩色马铃薯成为马铃薯产业的研究热点[2 -3 ] .植物中的花青素是一种天然水溶性色素,能使植物呈现出各种颜色[4 ] .马铃薯的薯肉通常呈白色或黄色,此外,紫色和红色等彩色马铃薯中的花青素含量相对较高.植物中花青素的合成代谢受到转录因子的调控,目前,已鉴定出3类参与花青素代谢合成的转录因子,分别为MYB家族成员、BHLH蛋白和WD40因子,其中R2R3-MYB为最主要的转录调控因子[5 ] . ...
彩色马铃薯查尔酮合酶基因的克隆及生物信息学分析
1
2022
... 我国马铃薯产业发展迅猛,随着生活水平的提升,人们对马铃薯食品的需求也逐渐从满足温饱向追求更高的营养保健价值转变[1 ] .花青素具有抗氧化、保护视力、降低心血管疾病风险以及提高人体免疫力及抗炎等功能,因而富含高花青素含量的彩色马铃薯成为马铃薯产业的研究热点[2 -3 ] .植物中的花青素是一种天然水溶性色素,能使植物呈现出各种颜色[4 ] .马铃薯的薯肉通常呈白色或黄色,此外,紫色和红色等彩色马铃薯中的花青素含量相对较高.植物中花青素的合成代谢受到转录因子的调控,目前,已鉴定出3类参与花青素代谢合成的转录因子,分别为MYB家族成员、BHLH蛋白和WD40因子,其中R2R3-MYB为最主要的转录调控因子[5 ] . ...
1
2016
... 我国马铃薯产业发展迅猛,随着生活水平的提升,人们对马铃薯食品的需求也逐渐从满足温饱向追求更高的营养保健价值转变[1 ] .花青素具有抗氧化、保护视力、降低心血管疾病风险以及提高人体免疫力及抗炎等功能,因而富含高花青素含量的彩色马铃薯成为马铃薯产业的研究热点[2 -3 ] .植物中的花青素是一种天然水溶性色素,能使植物呈现出各种颜色[4 ] .马铃薯的薯肉通常呈白色或黄色,此外,紫色和红色等彩色马铃薯中的花青素含量相对较高.植物中花青素的合成代谢受到转录因子的调控,目前,已鉴定出3类参与花青素代谢合成的转录因子,分别为MYB家族成员、BHLH蛋白和WD40因子,其中R2R3-MYB为最主要的转录调控因子[5 ] . ...
茄科植物花青素合成相关的MYB转录因子研究进展
1
2023
... MYB转录因子是植物中最大的一类转录因子家族,其重要的功能之一是调控花青素的合成[6 ] .MYB转录因子在结构上有一段位于N端的保守DNA结合区(MYB结构域),主要负责对靶基因上游启动子区域顺式作用元件的识别与结合[7 ] .MYB结构域通常是由不完全重复的氨基酸序列组成,重复序列R可分为R1、R2和R3,结构域之间的组合又可形成4种类型的MYB蛋白,分别为单-MYB结构域(R1/2、R3)蛋白、2R(R2R3)蛋白、3R(R1R2R3)蛋白和4R(R1R2R2R1/2)蛋白[8 ] ,广泛分布于植物中并发挥着重要的生物学功能,包括植物的生长发育、次级代谢调控和胁迫应答等.MYB转录因子还可以正向或负向调节花青素的生物合成[9 ] .史程程等[10 ] 采用RT-PCR方法在葡萄风信子中克隆获得1个MaMYB114 基因,对其进行生物信息学分析和异源转化烟草功能验证,表明其正向调控花青素合成.周薇[11 ] 从中华红叶杨中分离了花青素合成相关转录因子MYB118L 基因并对其蛋白序列特征、亚细胞定位、功能与作用机制进行探究,初步揭示了MYB118L 基因调控花青素合成过程的分子机制.鲁亚楠[12 ] 通过转录组和RT-PCR分析发现文冠果中的XsMYB113-1 、XsMYB113-2 、XsMYB113-3 和XsMYB113-4 基因均能正向调控花青素的合成.通过多个试验,不同植物中的MYB转录因子均被证实能够调控花青素合成,揭示了MYB转录因子在花青素生物合成途径中的关键作用. ...
MYB: an old oncoprotein with new roles
1
1995
... MYB转录因子是植物中最大的一类转录因子家族,其重要的功能之一是调控花青素的合成[6 ] .MYB转录因子在结构上有一段位于N端的保守DNA结合区(MYB结构域),主要负责对靶基因上游启动子区域顺式作用元件的识别与结合[7 ] .MYB结构域通常是由不完全重复的氨基酸序列组成,重复序列R可分为R1、R2和R3,结构域之间的组合又可形成4种类型的MYB蛋白,分别为单-MYB结构域(R1/2、R3)蛋白、2R(R2R3)蛋白、3R(R1R2R3)蛋白和4R(R1R2R2R1/2)蛋白[8 ] ,广泛分布于植物中并发挥着重要的生物学功能,包括植物的生长发育、次级代谢调控和胁迫应答等.MYB转录因子还可以正向或负向调节花青素的生物合成[9 ] .史程程等[10 ] 采用RT-PCR方法在葡萄风信子中克隆获得1个MaMYB114 基因,对其进行生物信息学分析和异源转化烟草功能验证,表明其正向调控花青素合成.周薇[11 ] 从中华红叶杨中分离了花青素合成相关转录因子MYB118L 基因并对其蛋白序列特征、亚细胞定位、功能与作用机制进行探究,初步揭示了MYB118L 基因调控花青素合成过程的分子机制.鲁亚楠[12 ] 通过转录组和RT-PCR分析发现文冠果中的XsMYB113-1 、XsMYB113-2 、XsMYB113-3 和XsMYB113-4 基因均能正向调控花青素的合成.通过多个试验,不同植物中的MYB转录因子均被证实能够调控花青素合成,揭示了MYB转录因子在花青素生物合成途径中的关键作用. ...
MYB transcription factors in Arabidopsis
1
2010
... MYB转录因子是植物中最大的一类转录因子家族,其重要的功能之一是调控花青素的合成[6 ] .MYB转录因子在结构上有一段位于N端的保守DNA结合区(MYB结构域),主要负责对靶基因上游启动子区域顺式作用元件的识别与结合[7 ] .MYB结构域通常是由不完全重复的氨基酸序列组成,重复序列R可分为R1、R2和R3,结构域之间的组合又可形成4种类型的MYB蛋白,分别为单-MYB结构域(R1/2、R3)蛋白、2R(R2R3)蛋白、3R(R1R2R3)蛋白和4R(R1R2R2R1/2)蛋白[8 ] ,广泛分布于植物中并发挥着重要的生物学功能,包括植物的生长发育、次级代谢调控和胁迫应答等.MYB转录因子还可以正向或负向调节花青素的生物合成[9 ] .史程程等[10 ] 采用RT-PCR方法在葡萄风信子中克隆获得1个MaMYB114 基因,对其进行生物信息学分析和异源转化烟草功能验证,表明其正向调控花青素合成.周薇[11 ] 从中华红叶杨中分离了花青素合成相关转录因子MYB118L 基因并对其蛋白序列特征、亚细胞定位、功能与作用机制进行探究,初步揭示了MYB118L 基因调控花青素合成过程的分子机制.鲁亚楠[12 ] 通过转录组和RT-PCR分析发现文冠果中的XsMYB113-1 、XsMYB113-2 、XsMYB113-3 和XsMYB113-4 基因均能正向调控花青素的合成.通过多个试验,不同植物中的MYB转录因子均被证实能够调控花青素合成,揭示了MYB转录因子在花青素生物合成途径中的关键作用. ...
引进马铃薯种质资源在干旱半干旱区的表型性状遗传多样性分析及综合评价
1
2018
... MYB转录因子是植物中最大的一类转录因子家族,其重要的功能之一是调控花青素的合成[6 ] .MYB转录因子在结构上有一段位于N端的保守DNA结合区(MYB结构域),主要负责对靶基因上游启动子区域顺式作用元件的识别与结合[7 ] .MYB结构域通常是由不完全重复的氨基酸序列组成,重复序列R可分为R1、R2和R3,结构域之间的组合又可形成4种类型的MYB蛋白,分别为单-MYB结构域(R1/2、R3)蛋白、2R(R2R3)蛋白、3R(R1R2R3)蛋白和4R(R1R2R2R1/2)蛋白[8 ] ,广泛分布于植物中并发挥着重要的生物学功能,包括植物的生长发育、次级代谢调控和胁迫应答等.MYB转录因子还可以正向或负向调节花青素的生物合成[9 ] .史程程等[10 ] 采用RT-PCR方法在葡萄风信子中克隆获得1个MaMYB114 基因,对其进行生物信息学分析和异源转化烟草功能验证,表明其正向调控花青素合成.周薇[11 ] 从中华红叶杨中分离了花青素合成相关转录因子MYB118L 基因并对其蛋白序列特征、亚细胞定位、功能与作用机制进行探究,初步揭示了MYB118L 基因调控花青素合成过程的分子机制.鲁亚楠[12 ] 通过转录组和RT-PCR分析发现文冠果中的XsMYB113-1 、XsMYB113-2 、XsMYB113-3 和XsMYB113-4 基因均能正向调控花青素的合成.通过多个试验,不同植物中的MYB转录因子均被证实能够调控花青素合成,揭示了MYB转录因子在花青素生物合成途径中的关键作用. ...
葡萄风信子Ma MYB114 基因的克隆及功能研究
1
2023
... MYB转录因子是植物中最大的一类转录因子家族,其重要的功能之一是调控花青素的合成[6 ] .MYB转录因子在结构上有一段位于N端的保守DNA结合区(MYB结构域),主要负责对靶基因上游启动子区域顺式作用元件的识别与结合[7 ] .MYB结构域通常是由不完全重复的氨基酸序列组成,重复序列R可分为R1、R2和R3,结构域之间的组合又可形成4种类型的MYB蛋白,分别为单-MYB结构域(R1/2、R3)蛋白、2R(R2R3)蛋白、3R(R1R2R3)蛋白和4R(R1R2R2R1/2)蛋白[8 ] ,广泛分布于植物中并发挥着重要的生物学功能,包括植物的生长发育、次级代谢调控和胁迫应答等.MYB转录因子还可以正向或负向调节花青素的生物合成[9 ] .史程程等[10 ] 采用RT-PCR方法在葡萄风信子中克隆获得1个MaMYB114 基因,对其进行生物信息学分析和异源转化烟草功能验证,表明其正向调控花青素合成.周薇[11 ] 从中华红叶杨中分离了花青素合成相关转录因子MYB118L 基因并对其蛋白序列特征、亚细胞定位、功能与作用机制进行探究,初步揭示了MYB118L 基因调控花青素合成过程的分子机制.鲁亚楠[12 ] 通过转录组和RT-PCR分析发现文冠果中的XsMYB113-1 、XsMYB113-2 、XsMYB113-3 和XsMYB113-4 基因均能正向调控花青素的合成.通过多个试验,不同植物中的MYB转录因子均被证实能够调控花青素合成,揭示了MYB转录因子在花青素生物合成途径中的关键作用. ...
1
2023
... MYB转录因子是植物中最大的一类转录因子家族,其重要的功能之一是调控花青素的合成[6 ] .MYB转录因子在结构上有一段位于N端的保守DNA结合区(MYB结构域),主要负责对靶基因上游启动子区域顺式作用元件的识别与结合[7 ] .MYB结构域通常是由不完全重复的氨基酸序列组成,重复序列R可分为R1、R2和R3,结构域之间的组合又可形成4种类型的MYB蛋白,分别为单-MYB结构域(R1/2、R3)蛋白、2R(R2R3)蛋白、3R(R1R2R3)蛋白和4R(R1R2R2R1/2)蛋白[8 ] ,广泛分布于植物中并发挥着重要的生物学功能,包括植物的生长发育、次级代谢调控和胁迫应答等.MYB转录因子还可以正向或负向调节花青素的生物合成[9 ] .史程程等[10 ] 采用RT-PCR方法在葡萄风信子中克隆获得1个MaMYB114 基因,对其进行生物信息学分析和异源转化烟草功能验证,表明其正向调控花青素合成.周薇[11 ] 从中华红叶杨中分离了花青素合成相关转录因子MYB118L 基因并对其蛋白序列特征、亚细胞定位、功能与作用机制进行探究,初步揭示了MYB118L 基因调控花青素合成过程的分子机制.鲁亚楠[12 ] 通过转录组和RT-PCR分析发现文冠果中的XsMYB113-1 、XsMYB113-2 、XsMYB113-3 和XsMYB113-4 基因均能正向调控花青素的合成.通过多个试验,不同植物中的MYB转录因子均被证实能够调控花青素合成,揭示了MYB转录因子在花青素生物合成途径中的关键作用. ...
1
2022
... MYB转录因子是植物中最大的一类转录因子家族,其重要的功能之一是调控花青素的合成[6 ] .MYB转录因子在结构上有一段位于N端的保守DNA结合区(MYB结构域),主要负责对靶基因上游启动子区域顺式作用元件的识别与结合[7 ] .MYB结构域通常是由不完全重复的氨基酸序列组成,重复序列R可分为R1、R2和R3,结构域之间的组合又可形成4种类型的MYB蛋白,分别为单-MYB结构域(R1/2、R3)蛋白、2R(R2R3)蛋白、3R(R1R2R3)蛋白和4R(R1R2R2R1/2)蛋白[8 ] ,广泛分布于植物中并发挥着重要的生物学功能,包括植物的生长发育、次级代谢调控和胁迫应答等.MYB转录因子还可以正向或负向调节花青素的生物合成[9 ] .史程程等[10 ] 采用RT-PCR方法在葡萄风信子中克隆获得1个MaMYB114 基因,对其进行生物信息学分析和异源转化烟草功能验证,表明其正向调控花青素合成.周薇[11 ] 从中华红叶杨中分离了花青素合成相关转录因子MYB118L 基因并对其蛋白序列特征、亚细胞定位、功能与作用机制进行探究,初步揭示了MYB118L 基因调控花青素合成过程的分子机制.鲁亚楠[12 ] 通过转录组和RT-PCR分析发现文冠果中的XsMYB113-1 、XsMYB113-2 、XsMYB113-3 和XsMYB113-4 基因均能正向调控花青素的合成.通过多个试验,不同植物中的MYB转录因子均被证实能够调控花青素合成,揭示了MYB转录因子在花青素生物合成途径中的关键作用. ...
不同栽培条件对马铃薯紫云1号花青素含量影响的研究
1
2010
... 在花青素合成调控中,MYB与bHLH、WD40单独作用,或者三者形成MBW复合体调控花青素的合成[13 ] .MYB与MYC转录因子bHLH具备结合活性,二者共同调控花青素合成晚期基因的表达[14 ] .本研究在马铃薯StMYB3蛋白序列中,发现了R2R3-MYB结构域的存在,这一结构域中还包含了与bHLH转录因子的相互作用.通过对不同品种和不同部位马铃薯StMYB3 基因的表达分析,发现该基因在嫩叶中表达最高,而且马铃薯StMYB3 基因在2013-89-61(薯肉深紫色)的根、茎、嫩叶和块茎中表达量均为最高,因此马铃薯StMYB3 基因可能参与马铃薯花青素合成的代谢路径.这与前人在研究马铃薯MYB转录因子的功能结果相近,例如,Lu等[15 ] 和Zhang等[16 ] 发现在马铃薯块茎中克隆到的R2R3-MYB转录因子中有共表达因子StbHLH1,在细胞核中表达且增强了MYB对花青素合成的调节作用.Jung等[17 ] 和许芸梅等[18 ] 对马铃薯红色薯肉基因进行了定位和筛选,发现其候选基因为R2R3-MYB转录因子,与控制薯皮花青素积累的StAN2 (D/I)相同.Liu等[19 ] 等研究了3个与R2R3- MYB转录因子(StAN1、StMYBA1和StMYB113)相关的功能,发现StMYBA1和StMYB113可以激活花青素的积累,且均具有部分R2R3结构域.而StbHLH1和StJAF13是花青素生物合成的关键共调节因子,StAN1、StMYBA1和StMYB113即使在没有色素积累的情况下也能表达.Rommens等[20 ] 发现MYB转录因子StMtf1 转基因植株基因激活了苯丙烷类生物合成路径,与对照相比,转基因块茎中的咖啡酰奎宁酸含量增加了4倍,包括绿原酸(CGA),同时也积累了黄酮醇和花青素.上述研究均表明MYB转录因子是花青素合成调控中的核心元件,其与其他转录因子的相互作用构成了调控花青素合成的关键机制.在马铃薯中,MYB转录因子不仅在马铃薯的花青素合成中发挥着关键作用,其还在不同组织(例如薯肉和薯皮)中具有调控作用.因此,马铃薯StMYB3 基因的更多功能需要亚细胞定位和转基因操作等进行进一步验证. ...
Characterization of the regulatory network of BoMYB2 in controlling anthocyanin biosynthesis in purple cauliflower
1
2012
... 在花青素合成调控中,MYB与bHLH、WD40单独作用,或者三者形成MBW复合体调控花青素的合成[13 ] .MYB与MYC转录因子bHLH具备结合活性,二者共同调控花青素合成晚期基因的表达[14 ] .本研究在马铃薯StMYB3蛋白序列中,发现了R2R3-MYB结构域的存在,这一结构域中还包含了与bHLH转录因子的相互作用.通过对不同品种和不同部位马铃薯StMYB3 基因的表达分析,发现该基因在嫩叶中表达最高,而且马铃薯StMYB3 基因在2013-89-61(薯肉深紫色)的根、茎、嫩叶和块茎中表达量均为最高,因此马铃薯StMYB3 基因可能参与马铃薯花青素合成的代谢路径.这与前人在研究马铃薯MYB转录因子的功能结果相近,例如,Lu等[15 ] 和Zhang等[16 ] 发现在马铃薯块茎中克隆到的R2R3-MYB转录因子中有共表达因子StbHLH1,在细胞核中表达且增强了MYB对花青素合成的调节作用.Jung等[17 ] 和许芸梅等[18 ] 对马铃薯红色薯肉基因进行了定位和筛选,发现其候选基因为R2R3-MYB转录因子,与控制薯皮花青素积累的StAN2 (D/I)相同.Liu等[19 ] 等研究了3个与R2R3- MYB转录因子(StAN1、StMYBA1和StMYB113)相关的功能,发现StMYBA1和StMYB113可以激活花青素的积累,且均具有部分R2R3结构域.而StbHLH1和StJAF13是花青素生物合成的关键共调节因子,StAN1、StMYBA1和StMYB113即使在没有色素积累的情况下也能表达.Rommens等[20 ] 发现MYB转录因子StMtf1 转基因植株基因激活了苯丙烷类生物合成路径,与对照相比,转基因块茎中的咖啡酰奎宁酸含量增加了4倍,包括绿原酸(CGA),同时也积累了黄酮醇和花青素.上述研究均表明MYB转录因子是花青素合成调控中的核心元件,其与其他转录因子的相互作用构成了调控花青素合成的关键机制.在马铃薯中,MYB转录因子不仅在马铃薯的花青素合成中发挥着关键作用,其还在不同组织(例如薯肉和薯皮)中具有调控作用.因此,马铃薯StMYB3 基因的更多功能需要亚细胞定位和转基因操作等进行进一步验证. ...
cDNA cloning and expression of anthocyanin biosynthetic genes in wild potato (Solanum pinnatisectum )
1
2006
... 在花青素合成调控中,MYB与bHLH、WD40单独作用,或者三者形成MBW复合体调控花青素的合成[13 ] .MYB与MYC转录因子bHLH具备结合活性,二者共同调控花青素合成晚期基因的表达[14 ] .本研究在马铃薯StMYB3蛋白序列中,发现了R2R3-MYB结构域的存在,这一结构域中还包含了与bHLH转录因子的相互作用.通过对不同品种和不同部位马铃薯StMYB3 基因的表达分析,发现该基因在嫩叶中表达最高,而且马铃薯StMYB3 基因在2013-89-61(薯肉深紫色)的根、茎、嫩叶和块茎中表达量均为最高,因此马铃薯StMYB3 基因可能参与马铃薯花青素合成的代谢路径.这与前人在研究马铃薯MYB转录因子的功能结果相近,例如,Lu等[15 ] 和Zhang等[16 ] 发现在马铃薯块茎中克隆到的R2R3-MYB转录因子中有共表达因子StbHLH1,在细胞核中表达且增强了MYB对花青素合成的调节作用.Jung等[17 ] 和许芸梅等[18 ] 对马铃薯红色薯肉基因进行了定位和筛选,发现其候选基因为R2R3-MYB转录因子,与控制薯皮花青素积累的StAN2 (D/I)相同.Liu等[19 ] 等研究了3个与R2R3- MYB转录因子(StAN1、StMYBA1和StMYB113)相关的功能,发现StMYBA1和StMYB113可以激活花青素的积累,且均具有部分R2R3结构域.而StbHLH1和StJAF13是花青素生物合成的关键共调节因子,StAN1、StMYBA1和StMYB113即使在没有色素积累的情况下也能表达.Rommens等[20 ] 发现MYB转录因子StMtf1 转基因植株基因激活了苯丙烷类生物合成路径,与对照相比,转基因块茎中的咖啡酰奎宁酸含量增加了4倍,包括绿原酸(CGA),同时也积累了黄酮醇和花青素.上述研究均表明MYB转录因子是花青素合成调控中的核心元件,其与其他转录因子的相互作用构成了调控花青素合成的关键机制.在马铃薯中,MYB转录因子不仅在马铃薯的花青素合成中发挥着关键作用,其还在不同组织(例如薯肉和薯皮)中具有调控作用.因此,马铃薯StMYB3 基因的更多功能需要亚细胞定位和转基因操作等进行进一步验证. ...
Genetic analysis of pigmented tuber flesh in potato
1
2009
... 在花青素合成调控中,MYB与bHLH、WD40单独作用,或者三者形成MBW复合体调控花青素的合成[13 ] .MYB与MYC转录因子bHLH具备结合活性,二者共同调控花青素合成晚期基因的表达[14 ] .本研究在马铃薯StMYB3蛋白序列中,发现了R2R3-MYB结构域的存在,这一结构域中还包含了与bHLH转录因子的相互作用.通过对不同品种和不同部位马铃薯StMYB3 基因的表达分析,发现该基因在嫩叶中表达最高,而且马铃薯StMYB3 基因在2013-89-61(薯肉深紫色)的根、茎、嫩叶和块茎中表达量均为最高,因此马铃薯StMYB3 基因可能参与马铃薯花青素合成的代谢路径.这与前人在研究马铃薯MYB转录因子的功能结果相近,例如,Lu等[15 ] 和Zhang等[16 ] 发现在马铃薯块茎中克隆到的R2R3-MYB转录因子中有共表达因子StbHLH1,在细胞核中表达且增强了MYB对花青素合成的调节作用.Jung等[17 ] 和许芸梅等[18 ] 对马铃薯红色薯肉基因进行了定位和筛选,发现其候选基因为R2R3-MYB转录因子,与控制薯皮花青素积累的StAN2 (D/I)相同.Liu等[19 ] 等研究了3个与R2R3- MYB转录因子(StAN1、StMYBA1和StMYB113)相关的功能,发现StMYBA1和StMYB113可以激活花青素的积累,且均具有部分R2R3结构域.而StbHLH1和StJAF13是花青素生物合成的关键共调节因子,StAN1、StMYBA1和StMYB113即使在没有色素积累的情况下也能表达.Rommens等[20 ] 发现MYB转录因子StMtf1 转基因植株基因激活了苯丙烷类生物合成路径,与对照相比,转基因块茎中的咖啡酰奎宁酸含量增加了4倍,包括绿原酸(CGA),同时也积累了黄酮醇和花青素.上述研究均表明MYB转录因子是花青素合成调控中的核心元件,其与其他转录因子的相互作用构成了调控花青素合成的关键机制.在马铃薯中,MYB转录因子不仅在马铃薯的花青素合成中发挥着关键作用,其还在不同组织(例如薯肉和薯皮)中具有调控作用.因此,马铃薯StMYB3 基因的更多功能需要亚细胞定位和转基因操作等进行进一步验证. ...
The potato developer(D) locus encodes an R2R3 MYB transcription factor that regulates expression of multiple anthocyanin structural genes in tuber skin
1
2009
... 在花青素合成调控中,MYB与bHLH、WD40单独作用,或者三者形成MBW复合体调控花青素的合成[13 ] .MYB与MYC转录因子bHLH具备结合活性,二者共同调控花青素合成晚期基因的表达[14 ] .本研究在马铃薯StMYB3蛋白序列中,发现了R2R3-MYB结构域的存在,这一结构域中还包含了与bHLH转录因子的相互作用.通过对不同品种和不同部位马铃薯StMYB3 基因的表达分析,发现该基因在嫩叶中表达最高,而且马铃薯StMYB3 基因在2013-89-61(薯肉深紫色)的根、茎、嫩叶和块茎中表达量均为最高,因此马铃薯StMYB3 基因可能参与马铃薯花青素合成的代谢路径.这与前人在研究马铃薯MYB转录因子的功能结果相近,例如,Lu等[15 ] 和Zhang等[16 ] 发现在马铃薯块茎中克隆到的R2R3-MYB转录因子中有共表达因子StbHLH1,在细胞核中表达且增强了MYB对花青素合成的调节作用.Jung等[17 ] 和许芸梅等[18 ] 对马铃薯红色薯肉基因进行了定位和筛选,发现其候选基因为R2R3-MYB转录因子,与控制薯皮花青素积累的StAN2 (D/I)相同.Liu等[19 ] 等研究了3个与R2R3- MYB转录因子(StAN1、StMYBA1和StMYB113)相关的功能,发现StMYBA1和StMYB113可以激活花青素的积累,且均具有部分R2R3结构域.而StbHLH1和StJAF13是花青素生物合成的关键共调节因子,StAN1、StMYBA1和StMYB113即使在没有色素积累的情况下也能表达.Rommens等[20 ] 发现MYB转录因子StMtf1 转基因植株基因激活了苯丙烷类生物合成路径,与对照相比,转基因块茎中的咖啡酰奎宁酸含量增加了4倍,包括绿原酸(CGA),同时也积累了黄酮醇和花青素.上述研究均表明MYB转录因子是花青素合成调控中的核心元件,其与其他转录因子的相互作用构成了调控花青素合成的关键机制.在马铃薯中,MYB转录因子不仅在马铃薯的花青素合成中发挥着关键作用,其还在不同组织(例如薯肉和薯皮)中具有调控作用.因此,马铃薯StMYB3 基因的更多功能需要亚细胞定位和转基因操作等进行进一步验证. ...
马铃薯红色薯肉调控基因的精细定位与候选基因分析
1
2019
... 在花青素合成调控中,MYB与bHLH、WD40单独作用,或者三者形成MBW复合体调控花青素的合成[13 ] .MYB与MYC转录因子bHLH具备结合活性,二者共同调控花青素合成晚期基因的表达[14 ] .本研究在马铃薯StMYB3蛋白序列中,发现了R2R3-MYB结构域的存在,这一结构域中还包含了与bHLH转录因子的相互作用.通过对不同品种和不同部位马铃薯StMYB3 基因的表达分析,发现该基因在嫩叶中表达最高,而且马铃薯StMYB3 基因在2013-89-61(薯肉深紫色)的根、茎、嫩叶和块茎中表达量均为最高,因此马铃薯StMYB3 基因可能参与马铃薯花青素合成的代谢路径.这与前人在研究马铃薯MYB转录因子的功能结果相近,例如,Lu等[15 ] 和Zhang等[16 ] 发现在马铃薯块茎中克隆到的R2R3-MYB转录因子中有共表达因子StbHLH1,在细胞核中表达且增强了MYB对花青素合成的调节作用.Jung等[17 ] 和许芸梅等[18 ] 对马铃薯红色薯肉基因进行了定位和筛选,发现其候选基因为R2R3-MYB转录因子,与控制薯皮花青素积累的StAN2 (D/I)相同.Liu等[19 ] 等研究了3个与R2R3- MYB转录因子(StAN1、StMYBA1和StMYB113)相关的功能,发现StMYBA1和StMYB113可以激活花青素的积累,且均具有部分R2R3结构域.而StbHLH1和StJAF13是花青素生物合成的关键共调节因子,StAN1、StMYBA1和StMYB113即使在没有色素积累的情况下也能表达.Rommens等[20 ] 发现MYB转录因子StMtf1 转基因植株基因激活了苯丙烷类生物合成路径,与对照相比,转基因块茎中的咖啡酰奎宁酸含量增加了4倍,包括绿原酸(CGA),同时也积累了黄酮醇和花青素.上述研究均表明MYB转录因子是花青素合成调控中的核心元件,其与其他转录因子的相互作用构成了调控花青素合成的关键机制.在马铃薯中,MYB转录因子不仅在马铃薯的花青素合成中发挥着关键作用,其还在不同组织(例如薯肉和薯皮)中具有调控作用.因此,马铃薯StMYB3 基因的更多功能需要亚细胞定位和转基因操作等进行进一步验证. ...
Functional diversification of the potato R2R3 MYB anthocyanin activators AN1, MYBA1, and MYB113 and their interaction with basic helixloop-helix cofactors
1
2016
... 在花青素合成调控中,MYB与bHLH、WD40单独作用,或者三者形成MBW复合体调控花青素的合成[13 ] .MYB与MYC转录因子bHLH具备结合活性,二者共同调控花青素合成晚期基因的表达[14 ] .本研究在马铃薯StMYB3蛋白序列中,发现了R2R3-MYB结构域的存在,这一结构域中还包含了与bHLH转录因子的相互作用.通过对不同品种和不同部位马铃薯StMYB3 基因的表达分析,发现该基因在嫩叶中表达最高,而且马铃薯StMYB3 基因在2013-89-61(薯肉深紫色)的根、茎、嫩叶和块茎中表达量均为最高,因此马铃薯StMYB3 基因可能参与马铃薯花青素合成的代谢路径.这与前人在研究马铃薯MYB转录因子的功能结果相近,例如,Lu等[15 ] 和Zhang等[16 ] 发现在马铃薯块茎中克隆到的R2R3-MYB转录因子中有共表达因子StbHLH1,在细胞核中表达且增强了MYB对花青素合成的调节作用.Jung等[17 ] 和许芸梅等[18 ] 对马铃薯红色薯肉基因进行了定位和筛选,发现其候选基因为R2R3-MYB转录因子,与控制薯皮花青素积累的StAN2 (D/I)相同.Liu等[19 ] 等研究了3个与R2R3- MYB转录因子(StAN1、StMYBA1和StMYB113)相关的功能,发现StMYBA1和StMYB113可以激活花青素的积累,且均具有部分R2R3结构域.而StbHLH1和StJAF13是花青素生物合成的关键共调节因子,StAN1、StMYBA1和StMYB113即使在没有色素积累的情况下也能表达.Rommens等[20 ] 发现MYB转录因子StMtf1 转基因植株基因激活了苯丙烷类生物合成路径,与对照相比,转基因块茎中的咖啡酰奎宁酸含量增加了4倍,包括绿原酸(CGA),同时也积累了黄酮醇和花青素.上述研究均表明MYB转录因子是花青素合成调控中的核心元件,其与其他转录因子的相互作用构成了调控花青素合成的关键机制.在马铃薯中,MYB转录因子不仅在马铃薯的花青素合成中发挥着关键作用,其还在不同组织(例如薯肉和薯皮)中具有调控作用.因此,马铃薯StMYB3 基因的更多功能需要亚细胞定位和转基因操作等进行进一步验证. ...
Engineered native pathways for high kaempferol and caffeoylquinate production in potato
1
2010
... 在花青素合成调控中,MYB与bHLH、WD40单独作用,或者三者形成MBW复合体调控花青素的合成[13 ] .MYB与MYC转录因子bHLH具备结合活性,二者共同调控花青素合成晚期基因的表达[14 ] .本研究在马铃薯StMYB3蛋白序列中,发现了R2R3-MYB结构域的存在,这一结构域中还包含了与bHLH转录因子的相互作用.通过对不同品种和不同部位马铃薯StMYB3 基因的表达分析,发现该基因在嫩叶中表达最高,而且马铃薯StMYB3 基因在2013-89-61(薯肉深紫色)的根、茎、嫩叶和块茎中表达量均为最高,因此马铃薯StMYB3 基因可能参与马铃薯花青素合成的代谢路径.这与前人在研究马铃薯MYB转录因子的功能结果相近,例如,Lu等[15 ] 和Zhang等[16 ] 发现在马铃薯块茎中克隆到的R2R3-MYB转录因子中有共表达因子StbHLH1,在细胞核中表达且增强了MYB对花青素合成的调节作用.Jung等[17 ] 和许芸梅等[18 ] 对马铃薯红色薯肉基因进行了定位和筛选,发现其候选基因为R2R3-MYB转录因子,与控制薯皮花青素积累的StAN2 (D/I)相同.Liu等[19 ] 等研究了3个与R2R3- MYB转录因子(StAN1、StMYBA1和StMYB113)相关的功能,发现StMYBA1和StMYB113可以激活花青素的积累,且均具有部分R2R3结构域.而StbHLH1和StJAF13是花青素生物合成的关键共调节因子,StAN1、StMYBA1和StMYB113即使在没有色素积累的情况下也能表达.Rommens等[20 ] 发现MYB转录因子StMtf1 转基因植株基因激活了苯丙烷类生物合成路径,与对照相比,转基因块茎中的咖啡酰奎宁酸含量增加了4倍,包括绿原酸(CGA),同时也积累了黄酮醇和花青素.上述研究均表明MYB转录因子是花青素合成调控中的核心元件,其与其他转录因子的相互作用构成了调控花青素合成的关键机制.在马铃薯中,MYB转录因子不仅在马铃薯的花青素合成中发挥着关键作用,其还在不同组织(例如薯肉和薯皮)中具有调控作用.因此,马铃薯StMYB3 基因的更多功能需要亚细胞定位和转基因操作等进行进一步验证. ...