作物杂志,2018, 第1期: 35–40 doi: 10.16035/j.issn.1001-7283.2018.01.005
高粱幼叶细胞悬浮系的建立
郝艳芳1,2,王良群1,2,刘勇1,张微1,2,杨伟1,白鸿雁1,武擘1
- 1 山西省农业科学院高粱研究所,030600,山西晋中
2 高粱遗传与种质创新山西省重点实验室,030600,山西晋中
Establishment of Sorghum Cell Suspensions with Young Leaves
Hao Yanfang1,2,Wang Liangqun1,2,Liu Yong1,Zhang Wei1,2,Yang Wei1,Bai Hongyan1,Wu Bo1
- 1 Sorghum Institute, Shanxi Academy of Agricultural Sciences, Jinzhong 030600, Shanxi, China
2 Shanxi Key Laboratory of Sorghum Genetic and Germplasm Innovation, Jinzhong 030600, Shanxi, China
摘要:
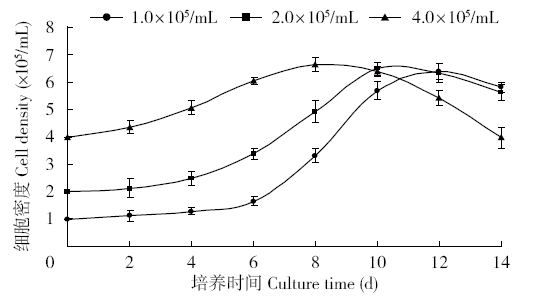
以高粱无菌苗幼叶为试验材料,对颗粒状胚性愈伤组织的获得、细胞悬浮系的建立及影响悬浮细胞生长的主要因素进行了研究。结果表明:幼叶在MS(Murashige and Skoog)+2mg/L 2,4-D培养基上诱导出的愈伤组织,经2~3次继代筛选后获得了浅黄色、颗粒状胚性愈伤组织;胚性愈伤组织接种于液体培养基中,于25±1℃、黑暗条件下,经45~60d的悬浮震荡培养建立了高质量的细胞悬浮系,细胞生长曲线呈“S”型,细胞密度可达6.45×10 5~5.08×10 6个/mL以上,活细胞率可达72.76%,近圆细胞率可达87.50%;培养基的基本成分、激素种类和水平对悬浮细胞生长状态有很大的影响,相比1/2MS培养基,MS培养基为适宜的培养基,2,4-D对保持细胞系的稳定增殖至关重要,适宜的浓度为1mg/L;培养液中加入0.5mg/L KT或6-BA会造成悬浮液褐化,影响悬浮细胞的生长;最适宜的细胞悬浮培养基为L2培养基(MS+1mg/L 2,4-D,30g/L蔗糖,pH5.8),震荡培养转速为110~120r/min,继代周期为7d,新旧培养基的接种比例为2∶1。
| [1] | 刘庆昌, 吴国良 . 植物细胞组织培养. 北京: 中国农业大学出版社, 2003: 139-162. |
| [2] | 杜晓映 . 葡萄细胞的悬浮培养及诱导子对悬浮细胞多酚产量影响的研究. 杨凌:西北农林科技大学, 2008. |
| [3] | 葛台明, 章荣德, 秦发兰 , 等. 冬小麦原生质体培养的胚状体直接发生. 生物工程学报, 2000,16(5):609-613. |
| [4] | 蔺忠龙, 白现广, 吕广磊 , 等. 疣粒野生稻胚性悬浮细胞系的建立及其原生质体的培养和植株再生. 植物生理学通讯, 2008,44(6):1181-1184. |
| [5] |
Xiang F N, Xia G M, Chen H M . Asymmetric somatic hybridization between wheat (Triticum aestivum) and Avena sativa L. Science in China Series C-Life Sciences, 2003,46(3):243-252.
doi: 10.1360/03yc9026 pmid: 18763139 |
| [6] |
Xiao W, Huang X, Gong Q , et al. Somatic hybrids obtained by asymmetric protoplast fusion between Musa Silk cv. Guoshanxiang (AAB) and Musa acuminata cv. Mas (AA). Plant Cell, Tissue and Organ Culture, 2009,97:313-321.
doi: 10.1007/s11240-009-9530-1 |
| [7] | Wagiran A, Ismail I, Zain C R , et al. Agrobacterium tumefaciens-mediated transformation of the isopentenyltransferase gene in japonica rice suspension cell culture. Australian Journal of Crop Science, 2010,4(6):421-429. |
| [8] |
Masteller V J, Holden D J . The growth of and organ formation from callus tissue of sorghum. Plant Physiology, 1970,45:362-364.
doi: 10.1104/pp.45.3.362 pmid: 16657320 |
| [9] |
Wernicke W, Brettel R I S . Morphogenesis from cultured leaf tissue of Sorghum bicolor-culture initiation. Protoplasma, 1982,111:19-27.
doi: 10.1007/BF01287643 |
| [10] |
Kumaravadivel N, Rangasamy S R S . Plant regeneration from sorghum anther cultures and field evaluation of progeny. Plant Cell Reports, 1994,13:286-290.
doi: 10.1007/BF00233321 pmid: 24193766 |
| [11] | Jogeswar G, Ranadheer D, Anjaiah V , et al. High frequency somatic embryogenesis and regeneration in different genotypes of Sorghum bicolor (L. ) Moench from immature inflorescence explants. In Vitro Cellular and Developmental Biology-Plant, 2007,43:159-166. |
| [12] |
Oldach C H, Morgenstern A, Rother S , et al. Efficient in vitro plant regeneration from immature zygotic embryos of pearl millet [Pennisetum glaucum (L.) R. Br. ] and Sorghum bicolor (L.) Moench. Plant Cell Reports, 2001,20:416-421.
doi: 10.1007/s002990100335 |
| [13] |
Kishore N S, Visarada K B R S,Lakshmi Y A , et al. In vitro culture methods in sorghum with shoot tip as the explant material. Plant Cell Reports, 2006,25:174-182.
doi: 10.1007/s00299-005-0044-y pmid: 16402251 |
| [14] |
Mythili P K, Seetharama N, Reddy V D . Plant regeneration from embryogenic cell suspension cultures of wild sorghum (Sorghum dimidiatum Stapf. ). Plant Cell Reports, 1999,18:424-428.
doi: 10.1007/s002990050597 |
| [15] |
王良群, 刘勇, 郝艳芳 , 等. 高粱茎尖和幼穗细胞悬浮系的建立. 农学学报, 2013,3(6):1-3.
doi: 10.3969/j.issn.1007-7774.2013.06.001 |
| [16] | 韩福光, 张颖 . 高粱不同外植体愈伤组织诱导的研究. 辽宁农业科学, 1993(1):45-48. |
| [17] |
王良群, 白志良, 王呈祥 , 等. 高粱不同外植体再生苗分化培养的研究. 杂粮作物, 2004,24(5):262-263.
doi: 10.3969/j.issn.2095-0896.2004.05.005 |
| [18] |
Baker C J, Mock N M . An improved method for monitoring cell death in cell suspension and leaf disc assays using evans blue. Plant Cell, Tissue and Organ Culture, 1994,39:7-12.
doi: 10.1007/BF00037585 |
| [19] |
赖钟雄, 陈振光 . 龙眼胚性细胞悬浮培养再生植株. 应用与环境生物学报, 2002,8(5):485-491.
doi: 10.3321/j.issn:1006-687X.2002.05.008 |
| [20] | 袁文娅, 关淑艳, 马红丹 , 等. 玉米自交系H99与齐319幼胚愈伤组织诱导条件的优化. 作物杂志, 2013(4):48-51. |
| [21] |
蔡汉权, 赖钟雄, 林珊珊, 等 . 罗勒 ( Ocimum basilicum)悬浮细胞系的建立与保持. 热带作物学报, 2006,27(1):44-48.
doi: 10.3969/j.issn.1000-2561.2006.01.009 |
| [22] | 欧巧明, 厚毅清, 包梅年 , 等. 中药半夏单细胞悬浮培养、胚胎发生及植株再生. 中国生物工程杂志, 2012,32(10):39-49. |
| [23] |
戴雪梅, 华玉伟, 李哲 , 等. 植物悬浮细胞培养的关键技术及存在问题. 热带生物学报, 2013,4(4):381-385.
doi: 10.3969/j.issn.1009-1823.2013.04.016 |
| [24] | 芦笛, 杨清, 陆巍 . 影响禾谷类作物胚性细胞悬浮系建立的一些因素. 植物生理学通讯, 2007,43(3):399-406. |
| [25] |
陈琰 . 不同抗叶锈小麦品种悬浮细胞系的建立. 保定:河北农业大学, 2005.
doi: 10.7666/d.y740357 |
| [26] |
乔妹 . 小麦“5389”悬浮细胞系的建立和植株再生. 保定:河北农业大学, 2011.
doi: 10.7666/d.y1897526 |
| [27] |
梁军, 魏刚, 吕全 , 等. 印楝细胞悬浮培养系的建立及悬浮培养. 林业科学研究, 2003,16(5):568-574.
doi: 10.3321/j.issn:1001-1498.2003.05.008 |
| [28] | 朱至清 . 植物细胞工程. 北京: 化学工业出版社, 2003: 25-26. |
| [29] | 方文娟, 韩烈保, 曾会明 . 植物细胞悬浮培养影响因子研究. 生物技术通报, 2005(5):11-15. |
| [1] | 张一中, 周福平 张晓娟 邵 强 杨 彬 柳青山. 高粱种质材料光合特性和水分#br# 利用效率鉴定及聚类分析[J]. 作物杂志, 2018, (5): 45–53 |
| [2] | 张瑞栋 曹 雄 岳忠孝 梁晓红 刘 静 黄敏佳. 氮肥和密度对高粱产量及氮肥利用率的影响[J]. 作物杂志, 2018, (5): 110–115 |
| [3] | 张建华 郭瑞峰 曹昌林 范 娜 江佰阳. 几种茎叶除草剂防除高粱田杂草药效和安全性研究[J]. 作物杂志, 2018, (5): 162–166 |
| [4] | 高杰,李青风,彭秋,焦晓燕,王劲松. 不同养分配比对糯高粱物质生产及氮磷钾利用效率的影响[J]. 作物杂志, 2018, (4): 138–142 |
| [5] | 张姣,吴奇,周宇飞,王艺陶,张瑞栋,黄瑞冬. 苗期和灌浆期干旱-复水对高粱光合特性和物质生产的影响[J]. 作物杂志, 2018, (3): 148–154 |
| [6] | 崔江辉,崔福柱,薛建福,郝建平,杜天庆,孙隆祥. 化肥减施对小麦-高粱系统土壤团聚体分布及其稳定性的影响[J]. 作物杂志, 2018, (1): 126–132 |
| [7] | 张微,王良群,刘勇,郝艳芳,杨伟,白鸿雁,武擘. 农杆菌介导高粱遗传转化的相关因素优化[J]. 作物杂志, 2018, (1): 56–61 |
| [8] | 朱凯,张飞,柯福来,王艳秋,邹剑秋. 种植密度对适宜机械化栽培高粱品种产量及生理特性的影响[J]. 作物杂志, 2018, (1): 83–87 |
| [9] | 高杰,李青风,汪灿,张国兵,彭秋. 不同氮素水平对糯高粱物质生产及氮素利用特性的影响[J]. 作物杂志, 2017, (6): 126–130 |
| [10] | 王聪,杨广东,胡尊艳,陈林祺,任思琪. 种植密度对高粱冠层结构及光辐射特征的影响[J]. 作物杂志, 2017, (5): 119–123 |
| [11] | 丁超,张建华,白文斌,郭瑞峰,曹昌林. 高粱田常用除草剂对高粱生理生化及产量品质的影响[J]. 作物杂志, 2017, (5): 149–155 |
| [12] | 于纪珍,王瑞,詹鹏杰,平俊爱,张福耀. 中国主要高粱杂交种农艺及品质性状多样性分析[J]. 作物杂志, 2017, (5): 49–54 |
| [13] | 张伟,张阳,赵威军,邵荣峰,卜华虎,常玉卉,李金梅,王花云. 烯效唑对甜高粱农艺性状及倒伏率的影响[J]. 作物杂志, 2017, (4): 113–116 |
| [14] | 张晓娟,周福平,张一中,邵强,范昕琦,刘勇,柳青山. 复粒高粱不育系的研究[J]. 作物杂志, 2017, (2): 72–75 |
| [15] | 王欢,刘冰,白子裕,史俊丽,叶锦琳. 激光辐射和杂交对高粱DNA甲基化变异的影响[J]. 作物杂志, 2017, (1): 32–37 |
|