苦荞[Fagopyrum tataricum (L.) Gaertn.]属蓼科(Polygonaceae)荞麦属(Fagopyrum Mill.),为一年生双子叶草本植物,是荞麦的2个栽培种之一[1]。我国是苦荞的起源地与集中分布区,种植历史悠久,种植面积和产量均居世界前列[2]。苦荞具有生育期短、抗旱、耐冷凉、耐贫瘠和适应性较强等特性[3],主要分布于我国西南、华北和西北等地区[4-5]。作为一种典型的药食同源小宗作物[6],苦荞不仅富含蛋白质、氨基酸、脂肪、膳食纤维、维生素和矿质元素等营养物质,还含有生物类黄酮、皂苷和D-手性肌醇等生物活性物质,具备消炎、抗氧化、抗动脉硬化、降“三高”、防治糖尿病及防癌抗癌等多种医药保健功效[7
种质资源收集与评价是作物育种工作的基础,利用分子标记技术开展苦荞种质资源遗传多样性及亲缘关系研究,对苦荞新品种选育与产业发展具有重要意义。简单重复序列(simple sequence repeat,SSR)分子标记因操作简便、多态性丰富且重复性高,在近似品种鉴别方面优势突出,成为当前研究首选的分子标记之一,已广泛应用于水稻[12]、小麦[13]和玉米[14]等主要作物的遗传多样性研究。随着苦荞全基因组及转录组测序数据的公布[15],SSR分子标记在苦荞种质资源研究中的应用愈发广泛。目前,国内已有一些使用SSR分子标记技术开展苦荞遗传多样性研究的报道,冷宇鑫等[16]采用SSR分子标记对60份贵州荞麦种质进行遗传多样性分析,构建了DNA分子身份证数据库,证实贵州省荞麦种质资源遗传多样性丰富;李晓瑜等[17]以318份苦荞种质资源为材料,利用SSR分子标记对11个农艺性状进行关联分析,检测到54个SSR标记与苦荞种质资源农艺性状极显著关联,为苦荞杂交组合亲本选配及分子标记辅助育种提供了依据;蔡齐宗等[5]验证了苦荞基因组富含SSR位点,其中单核苷酸重复和二核苷酸重复类型最为丰富,SSR位点平均距离为3.04 kb,开发的SSR分子标记多态性良好;左茜茜等[6]挖掘苦荞8条染色体基因组序列的SSR标记,发现42份苦荞地方品种资源多样性较高,验证了云贵川地区苦荞种质资源遗传多样性普遍高于其他区域的结论[18-
本研究采用SSR分子标记对104份不同来源的苦荞种质资源开展遗传多样性与群体结构分析,旨在揭示苦荞种质资源之间的遗传关系,探明苦荞资源与地域分布之间的关系,筛选出亲缘关系较单一的种质资源,为苦荞种质资源的进一步有效利用及新品种选育提供理论依据。
1 材料与方法
1.1 供试材料
供试材料选自内蒙古自治区农牧业科学院作物科学研究所收集保存的苦荞种质资源,共计104份。其中25份来源于内蒙古,79份来源于四川、贵州、云南和重庆等9个省份(表1)。
表1 供试材料信息
Table 1
| 材料编号 Material number | 来源地 Origin | 材料编号 Material number | 来源地 Origin | 材料编号 Material number | 来源地 Origin | 材料编号 Material number | 来源地 Origin | 材料编号 Material number | 来源地 Origin |
|---|---|---|---|---|---|---|---|---|---|
| S1 | 江西 | S32 | 云南 | S60 | 贵州 | S83 | 重庆 | S110 | 四川 |
| S4 | 四川 | S34 | 云南 | S61 | 贵州 | S84 | 内蒙古 | S111 | 四川 |
| S5 | 山西 | S35 | 贵州 | S62 | 贵州 | S85 | 内蒙古 | S112 | 四川 |
| S7 | 贵州 | S36 | 四川 | S63 | 贵州 | S86 | 内蒙古 | S113 | 四川 |
| S10 | 四川 | S37 | 甘肃 | S64 | 陕西 | S87 | 内蒙古 | S114 | 四川 |
| S12 | 四川 | S38 | 甘肃 | S65 | 陕西 | S91 | 内蒙古 | S115 | 四川 |
| S13 | 四川 | S39 | 甘肃 | S66 | 陕西 | S92 | 内蒙古 | S116 | 四川 |
| S14 | 贵州 | S40 | 陕西 | S67 | 陕西 | S93 | 内蒙古 | S117 | 四川 |
| S15 | 贵州 | S42 | 云南 | S68 | 陕西 | S94 | 内蒙古 | S118 | 四川 |
| S17 | 湖南 | S43 | 云南 | S69 | 陕西 | S95 | 山西 | S119 | 四川 |
| S18 | 山西 | S44 | 云南 | S70 | 云南 | S96 | 重庆 | S120 | 四川 |
| S20 | 山西 | S45 | 贵州 | S71 | 云南 | S97 | 重庆 | S122 | 内蒙古 |
| S22 | 甘肃 | S46 | 贵州 | S72 | 内蒙古 | S99 | 重庆 | S125 | 内蒙古 |
| S23 | 山西 | S47 | 四川 | S74 | 内蒙古 | S100 | 重庆 | S127 | 甘肃 |
| S24 | 云南 | S48 | 四川 | S75 | 内蒙古 | S102 | 贵州 | S128 | 内蒙古 |
| S25 | 云南 | S49 | 贵州 | S76 | 内蒙古 | S104 | 重庆 | S129 | 内蒙古 |
| S26 | 云南 | S50 | 贵州 | S77 | 内蒙古 | S105 | 重庆 | S130 | 内蒙古 |
| S27 | 云南 | S53 | 贵州 | S78 | 内蒙古 | S106 | 重庆 | S143 | 内蒙古 |
| S28 | 云南 | S54 | 贵州 | S79 | 内蒙古 | S107 | 重庆 | S147 | 内蒙古 |
| S29 | 云南 | S55 | 云南 | S80 | 内蒙古 | S108 | 内蒙古 | S148 | 甘肃 |
| S30 | 云南 | S56 | 四川 | S82 | 陕西 | S109 | 内蒙古 |
1.2 苦荞基因组DNA的提取
每份材料取15粒种子播种于育苗盘中。待种子长出2片子叶后,随机采集3个单株,每株取1片子叶混合,液氮速冻后迅速研磨成粉末状,采用CTAB法[22]提取基因组DNA。利用1%琼脂糖凝胶电泳初步检测所提取DNA的大小和质量,再用紫外分光光度计检测DNA的质量浓度,根据A260和A280处吸光度的比值检测DNA质量,将DNA样本置于-80 ℃条件保存。
1.3 SSR引物设计及多态性检测
利用Primer Express 3.0软件对SSR引物进行批量设计,随机选取100对设计的引物送至生工生物工程(上海)股份有限公司进行引物合成。选取表型差异较大的15份材料DNA(S1、S4、S5、S7、S10、S12、S13、S14、S15、S17、S18、S20、S22、S23和S24)作为PCR扩增模板,用于验证引物的多态性。PCR反应总体积为10 μL,包含5 μL 2×Taq PCR Master Mix(南京诺唯赞生物科技股份有限公司),正向引物(10 µmol/L)1.0 μL,反向引物(10 µmol/L)1.0 μL,DNA模板1.0 μL和2.0 μL ddH2O。PCR扩增反应程序:95 ℃预变性2 min;94 ℃变性40 s,56 ℃退火45 s,72 ℃延伸1 min,27个循环;最后72 ℃延伸7 min。反应结束后,在产物中加入2 μL缓冲液(0.5×TBE)并离心,以50~500 bp DNA分子量为标准,利用毛细管电泳,对扩增产物进行多态性检测。从具有多态性的引物中选择多态性最高的9对作为参试引物。采用6%~8%的非变性聚丙烯酰胺凝胶电泳,电泳缓冲液为0.5×TBE,左右端空格避免边缘效应,电泳上样量1.5 µL,两端各设置1个50 bp标记,电泳条件为:首先在120 V、400 mA下运行20 min,随后在180 V、400 mA下运行1 h 20 min,扩增片段移动至凝胶中部时停止电泳。取出凝胶后用银染法染色,并将其放置在凝胶成像仪上拍照观察。
1.4 数据处理
根据SSR扩增产物在电泳凝胶上的迁移位置,人工判读条带,有扩增条带记为“1”,无扩增条带记为“0”,构建二元数据矩阵,并计算多态性条带百分率。利用GenAlEx 6.51b2软件分析单个SSR位点在样本整体的等位基因数(Na)、有效等位基因数(Ne)、Shannon’s多样性指数(I)、观测杂合度(Ho)和期望杂合度(He)。
使用Structure 2.3.1软件分析供试材料的群体遗传结构,将群体数目预测值K设置为1~20,MCMC(Markov chain Monte Carlo)和不作数迭代次数分别设置为50 000和100 000,每个K值重复运行20次;将运行结果导入在线程序structure Harvester(
利用GenALEx 6.51b2软件计算遗传距离矩阵,在此基础上进行二维主坐标分析,并绘制前2个主成分的PCoA(principal coordinates analysis)二维散点图。
2 结果与分析
2.1 SSR引物的多态性分析
从100对SSR引物中筛选出9对条带清晰且多态性较好的引物。扩增结果(表2)显示,9对引物在104份苦荞种质资源中共扩增出22个等位基因,每对引物扩增等位基因数在2~4范围内,平均每个位点为2.444个。有效等位基因数的平均值为1.820;Shannon’s多样性指数范围为0.031~1.204,平均值为0.629;P99的观测杂合度最大,为0.106,P13和P52最小(0.010);期望杂合度的变化范围为0.010~0.675,平均值为0.401;9对引物的PIC范围为0.0096~0.6115,其中P21最高,为0.6115,P52最低,为0.0096。本研究中,筛选出的9对引物检测104份苦荞种质资源的平均PIC值为0.3312,说明种质遗传基础较丰富,呈中度多态性。
表2 SSR引物扩增多态性信息
Table 2
| 引物 Primer | 引物序列(5’→3’) Primer sequence | 等位 基因数 Na | 有效等位 基因数 Ne | Shannon’s 多样性指数 I | 观测 杂合度 Ho | 期望 杂合度 He | 多态性 信息含量 PIC |
|---|---|---|---|---|---|---|---|
| P13 | F:AAATTTCGGGCATAGATTCTGA | 2 | 1.413 | 0.468 | 0.010 | 0.292 | 0.2497 |
| R:TTCGATCCATCTTTTGGGAG | |||||||
| P21 | F:ACTCTTCCTCAGCGCTTCAC | 4 | 3.081 | 1.204 | 0.077 | 0.675 | 0.6115 |
| R:TCCTTGCCTAGTCCAGCAGT | |||||||
| P43 | F:AATTTGTTGGCACACAAGCA | 3 | 1.420 | 0.506 | 0.048 | 0.296 | 0.2573 |
| R:GTTGGGACAAGAAGGACTCG | |||||||
| P52 | F:CGATCCCGTAAGATCTCGTC | 2 | 1.010 | 0.031 | 0.010 | 0.010 | 0.0096 |
| R:CGAGTTTCGAACTCCTGACC | |||||||
| P53 | F:TCCATGTTTGAGGGGCTAAG | 3 | 2.086 | 0.870 | 0.058 | 0.521 | 0.4499 |
| R:AAATTCTTGCGCATTGCATA | |||||||
| P68 | F:AAGGGCAAGATTGCTTACCA | 2 | 1.874 | 0.659 | 0.087 | 0.466 | 0.3576 |
| R:GTCAGGATCCATTGTGGGAT | |||||||
| P69 | F:AAGGCAAGGGTATAAAGGGAA | 2 | 1.649 | 0.582 | 0.077 | 0.393 | 0.3161 |
| R:GAACAGGAACCCGAATACGA | |||||||
| P76 | F:CATACACATCCGCCAACAAG | 2 | 1.969 | 0.685 | 0.048 | 0.492 | 0.3711 |
| R:GTTAAGGCAAACTCGGTCCA | |||||||
| P99 | F:AGTGAAATTTTGGTGGACGC | 2 | 1.874 | 0.659 | 0.106 | 0.466 | 0.3576 |
| R:TCGTACTTTCCAAACGCTACA | |||||||
| 平均值Mean | 2.444 | 1.820 | 0.629 | 0.058 | 0.401 | 0.3312 | |
2.2 苦荞种质资源UPGMA聚类分析
图1
图1
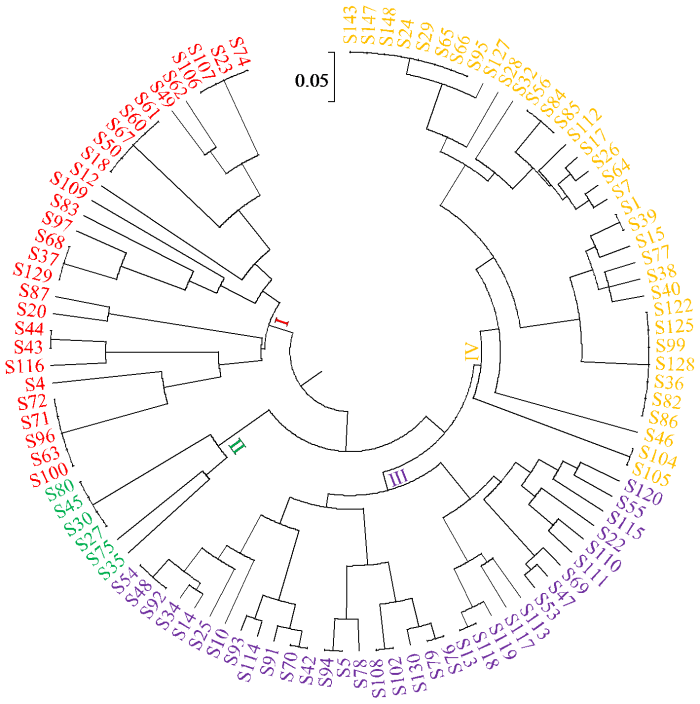
104份苦荞种质资源UPGMA聚类分析
Fig.1
UPGMA cluster analysis of 104 tartary buckwheat germplasm resources
表3 基于UPGMA聚类分析划分的4个组群种质构成
Table 3
| 组群 Group | 种质总数 Total germplasms | 比例 Percentage (%) | 种质来源(数量) Origin of germplasms (number) |
|---|---|---|---|
| Ⅰ | 29 | 27.89 | 甘肃(1);贵州(6);内蒙古(5);山西(3);陕西(2);四川(3);云南(3);重庆(6) |
| Ⅱ | 6 | 5.77 | 贵州(2);内蒙古(2);云南(2) |
| Ⅲ | 34 | 32.69 | 甘肃(1);贵州(4);内蒙古(9);山西(1);陕西(1);四川(13);云南(5) |
| Ⅳ | 35 | 33.65 | 甘肃(4);贵州(3);湖南(1);江西(1);内蒙古(9);山西(1);陕西(5);四川(3);云南(5);重庆(3) |
2.3 苦荞种质资源群体结构分析
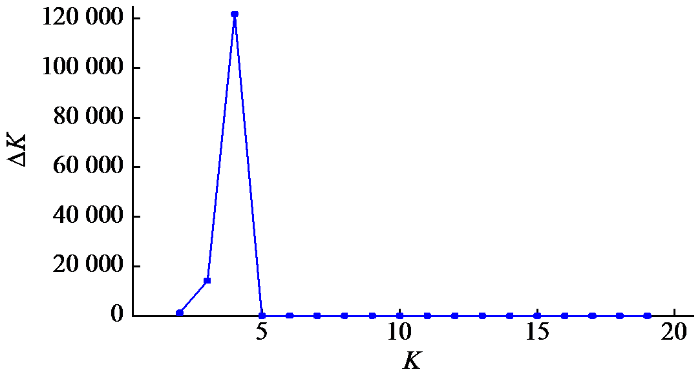
对供试材料进行群体结构分析(图2),当K=4时∆K出现最大值,由此判断可将104份苦荞种质资源划分为4个组群。K=4时的群体遗传结构如图3所示,4个组群分别命名为A、B、C和D,表4为各组群中资源来源情况,表5为104份材料在各组群中的Q值分布。104份资源材料中有20份Q值<0.6,84份Q值≥0.6,说明各组群中大多数资源材料亲缘关系相对单一。组群B中Q值≥0.9的材料数共17份(S18、S23、S49、S50、S60、S61、S62、S63、S67、S71、S72、S74、S96、S97、S100、S106和S107),占组群B种质总数的85%,为4个组群中Q值≥0.9种质占比最高的组群,说明组群B中的材料亲缘关系最为单一。与UPGMA聚类分析对比,组群Ⅰ与组群B中有19份材料相同,组群Ⅱ与组群D中有5份材料相同,组群Ⅲ与组群D中有25份材料相同,组群Ⅳ与组群A和组群C中分别有14和19份材料相同,群体结构分析与聚类分析结果基本一致。
图2
图3
图3
104份苦荞种质资源群体遗传结构(K=4)
Fig.3
Population genetic structure of 104 tartary buckwheat germplasm resources (K=4)
表4 基于群体结构分析划分的4个组群种质构成
Table 4
| 组群 Group | 种质总数 Total germplasms | 比例 Percentage (%) | 种质来源(数量) Origin of germplasms (number) |
|---|---|---|---|
| A | 25 | 24.04 | 甘肃(3);贵州(1);江西(1);内蒙古(11);陕西(3);四川(2);云南(2);重庆(2) |
| B | 20 | 19.23 | 贵州(7);内蒙古(3);山西(2);陕西(1);四川(1);云南(1);重庆(5) |
| C | 23 | 22.12 | 甘肃(3);贵州(2);湖南(1);内蒙古(5);山西(1);陕西(3);四川(3);云南(3);重庆(2) |
| D | 36 | 34.61 | 贵州(5);内蒙古(6);山西(2);陕西(1);四川(13);云南(9) |
表5 基于群体结构分析划分的4个组群Q值分布
Table 5
| 组群 Group | 种质总数 Total germplasms | 种质数量Number of germplasms | |||
|---|---|---|---|---|---|
| Q<0.6 | 0.6≤Q<0.8 | 0.8≤Q<0.9 | Q≥0.9 | ||
| A | 25 | 6 | 19 | 12 | 7 |
| B | 20 | 2 | 18 | 17 | 17 |
| C | 23 | 5 | 18 | 10 | 9 |
| D | 36 | 7 | 29 | 14 | 7 |
2.4 苦荞种质SSR标记的二维主坐标分析(PCoA)
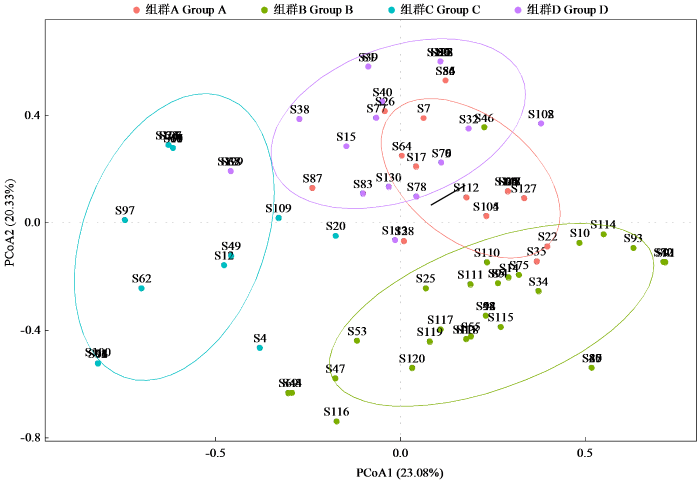
对104份苦荞种质资源的SSR标记分析数据进行二维主坐标分析(图4),将供试材料划分为4个部分,划分结果与群体结构划分的4个组群一一对应,其中紫色部分对应组群A,蓝色部分对应组群B,红色部分对应组群C,绿色部分对应组群D,此结果进一步验证了群体结构分析的准确性。
图4
图4
104份苦荞种质资源的主坐标分析二维散点图
Fig.4
Principal coordinate analysis two-dimensional scatter plot of 104 tartary buckwheat germplasm resources
3 讨论
亲本材料的选择以及育种材料遗传多样性与亲缘关系的明确,对育种工作至关重要。本研究采用15份苦荞材料对100对合成SSR引物进行多态性分析,结果显示58对引物呈现多态性,占比达58%。经优化筛选,最终选定9对引物对104份苦荞种质资源进行PCR扩增,扩增所得PIC范围为0.0096~0.6115,平均值为0.3312,表明104份苦荞种质资源遗传基础较为丰富,呈中度多态性。该数值低于高帆等[18]和冷宇鑫等[16]所得苦荞SSR标记的PIC平均值(分别为0.88和0.69),与李晓瑜等[17]和李春花等[26]所得苦荞SSR标记的PIC平均值(分别为0.46和0.34)基本相当,这可能与材料和SSR引物选择差异以及检测方法不同有关。
本研究运用UPGMA聚类分析方法,将104份苦荞种质资源划分为4个组群。从地理来源角度分析,内蒙古、云南、贵州和四川的苦荞种质分布情况相似,主要集中于组群Ⅲ和Ⅳ,表明内蒙古与云贵川地区的苦荞亲缘关系较近,其余省份的苦荞种质分布相对均匀,说明可能存在同物异名情况。综上,104份苦荞种质资源具有较为丰富的遗传多样性。通过群体遗传结构分析,104份苦荞种质资源同样被划分为4个组群,其中组群A含25份种质,组群B含20份,组群C含23份,组群D含36份。进一步分析发现,组群Ⅰ与组群B有19份种质重合,组群Ⅱ与组群D有5份重合,组群Ⅲ与组群D有25份重合,组群Ⅳ与组群A、组群C分别有14份、19份种质重合。在104份种质资源中,20份Q值<0.6,84份Q值≥0.6,表明各组群内多数资源材料的亲缘关系相对单一,基因渗透较少。其中,组群B中有17份种质(S18、S23、S49、S50、S60、S61、S62、S63、S67、S71、S72、S74、S96、S97、S100、S106和S107)Q值≥0.9,占组群B材料总数的85%,为4个组群中Q值≥0.9种质占比最高者,显示出这17份种质亲缘关系极为单一,适合作为后期亲本筛选及新品种选育的材料。
采用二维主坐标分析(PCoA)对群体遗传结构进行验证,结果基本一致。组群B中的资源材料均位于蓝色区域内,与其他区域几乎无重叠,证明组群B内种质资源亲缘关系单一,且与其他组群材料亲缘关系较远。
4 结论
104份苦荞地方种质遗传基础较丰富,呈中度多态性,内蒙古与云贵川苦荞亲缘关系较近。筛选出17份(S18、S23、S49、S50、S60、S61、S62、S63、S67、S71、S72、S74、S96、S97、S100、S106和S107)亲缘关系单一的种质资源,后续可用于亲本筛选,有助于培育优良的后代杂交创新品种。
参考文献
Buckwheat: origins and development
苦荞全基因组SSR位点挖掘及遗传多样性分析
DOI:10.13304/j.nykjdb.2021.0521
[本文引用: 2]

苦荞是一种重要的杂粮作物。利用GenBank数据库中苦荞的8条染色体基因组序列进行SSR标记挖掘,并基于Primer 3.0设计SSR引物,筛选多态性高的引物进行遗传多样性评价。共检测到51 485个SSR 位点,平均发生频率为114.07 Mb<sup>-1</sup>,二核苷酸重复型最多(78.20%),其次为三核苷酸重复型(17.76%)。苦荞SSR中包含361种类型重复基元,具有碱基偏好性,优势基元为AT/TA (69.60%)、AAT/TTA (2.49 %)和AGA/TCT(2.10 %)。序列长度变化范围为12~228 bp,长度12~20 bp的占比57.93 %,长度大于20 bp 的占比42.07 %。SSR位点分布在每条染色体上的数量和种类特征较为一致,不同染色体能检出的SSR种类具有特异性。根据不同类型SSR位点设计并合成156对引物,筛选出17对多态性较高的引物用于遗传多样性分析,发现42份苦荞地方品种资源具有较高的多样性,美姑县的黑苦荞遗传多样性最高,布拖县的样品多数聚为同一分支,多样性显著低于美姑县和昭觉县的品种,西南种质库保存的野生苦荞与其他栽培品种明显分离。通过大量SSR的挖掘特别是染色体特异性SSR位点的挖掘,对苦荞种质资源的鉴定分析以及苦荞分子标记辅助育种有重要意义;遗传多样性检测也显示了SSR分子标记的可用性,以及黑苦荞的遗传多样性水平,对苦荞遗传多样性保护研究提供了新的途径。
Effects of nitrogen level on the physicochemical properties of Tartary buckwheat (Fagopyrum tataricum (L.) Gaertn.) starch
苦荞麦化学成分及药理活性研究进展
自交可育甜荞、金苦荞、米苦荞不同品系总黄酮、粗蛋白及其蛋白组分含量研究
山西省代县药用植物资源调查研究
The tartary buckwheat genome provides insights into rutin biosynthesis and abiotic stress tolerance
DOI:10.1016/j.molp.2017.08.013 URL [本文引用: 1]
苦荞种质资源主要农艺性状SSR标记关联分析
DOI:10.3724/SP.J.1006.2022.11113
[本文引用: 2]

分析苦荞(Fagopyrum tataricum)种质资源遗传多样性和群体遗传结构, 筛选与苦荞农艺性状关联的分子标记, 为苦荞杂交组合的亲本选配及分子标记辅助育种提供依据。本试验以318份苦荞种质资源为材料, 分别于2019年和2020年对其主要农艺性状(株高、主茎分枝数、主茎节数和千粒重)及籽粒特征值(粒长、粒宽、籽粒长宽比、籽粒面积、籽粒周长、籽粒直径、籽粒圆度)进行了表型鉴定, 并通过分析2年的表型数据计算出BLUP值。77对具有良好多态性的SSR标记扫描群体, 共检测到293个等位变异, 基因多样性均值为0.52, PIC值平均为0.46; 聚类分析将318份苦荞资源分成4大类, 平均遗传距离0.44; 群体结构分析表明该群体可分为2个亚群。上述SSR标记分别对这11个表型性状进行了关联分析, 共检测有54个SSR标记与苦荞种质资源农艺性状极显著关联, 表型变异解释率为1.77%~16.40%, 其中25个标记在3个环境中均检测到, 47个SSR标记同时和2个或以上的表型性状呈极显著关联。该研究结果对苦荞相关性状的候选基因挖掘和高产苦荞分子标记辅助育种具有重要意义。
中国苦荞SSR分子标记体系构建及其在遗传多样性分析中的应用
DOI:10.3864/j.issn.0578-1752.2012.06.002
[本文引用: 2]

【目的】从分子水平优化并构建用于中国苦荞种质资源遗传多样性分析的SSR分子标记体系,为综合评价中国苦荞种质资源提供依据。【方法】以50份苦荞种质为试验材料,用正交设计法[L16(45)]筛选适用于苦荞SSR标记分析的PCR反应体系,浓度梯度检测最佳胶分离效果,并从250对不同科属作物SSR引物中筛选出19对引物进行苦荞遗传多样性分析。【结果】优化的苦荞SSR反应体系为DNA模板30 ng,Taq酶2.0 U•L-1,dNTP、引物和Mg2+终浓度分别为150 μmol•L-1、0.1 μmol•L-1、2.0 mmol•L-1,总体积为25 μL,6%聚丙烯酰胺凝胶电泳检测。SSR引物筛选率为7.6%,蓼科同属甜荞的SSR引物适用于苦荞SSR扩增。19对引物共检测到157个等位变异,每对SSR引物检测到的等位变异2—11个,平均等位变异(NA)7.42个,平均多态性信息量(PIC)0.888,平均鉴定力(DP)5.684,2对为SSR骨干引物。利用Popgen Ver.1.31软件,当遗传相似度(GS)为0.578时,50份苦荞材料被分为5个组群,聚类结果与苦荞地理分布相关性不大。四川苦荞资源组群各遗传多样性参数均最高,该区域苦荞种质资源多样性最丰富。利用骨干引物可鉴定部分近缘苦荞品种。【结论】构建的SSR分子标记体系适用于中国苦荞种质资源遗传多样性分析,甜荞SSR引物可用于苦荞SSR标记分析,TBP5和Fes2695为苦荞SSR骨干引物,50份苦荞材料遗传多样性丰富,可划分为5个组群。
104份苦荞种质的遗传多样性分析
A rapid DNA isolation procedure for small quantities of fresh leaf tissue
110份普通玉米自交系的SSR聚类分析
DOI:10.7668/hbnxb.2014.06.018
[本文引用: 1]

为了明确110份玉米自交系的亲缘关系,更好地利用和改良玉米自交系,以代表国内主要杂种优势群的4个标准测验种(丹340、黄早4、Mo17、K12)与106份普通玉米自交系为材料,利用SSR分子标记进行遗传多样性分析,选用28对SSR引物对供试材料进行了遗传多样性研究。结果表明,在供试材料中共检测到125个等位基因变异,平均每对引物检测到的等位基因变异为4.46个,变异为2~10个, 平均多态性信息量PIC值为0.85,变化范围为0.75~0.94。利用UPGMA聚类分析方法可将110份普通玉米自交系划分为6个类群。
Construction of a genetic linkage map in man using restriction fragment length polymorphisms
We describe a new basis for the construction of a genetic linkage map of the human genome. The basic principle of the mapping scheme is to develop, by recombinant DNA techniques, random single-copy DNA probes capable of detecting DNA sequence polymorphisms, when hybridized to restriction digests of an individual's DNA. Each of these probes will define a locus. Loci can be expanded or contracted to include more or less polymorphism by further application of recombinant DNA technology. Suitably polymorphic loci can be tested for linkage relationships in human pedigrees by established methods; and loci can be arranged into linkage groups to form a true genetic map of "DNA marker loci." Pedigrees in which inherited traits are known to be segregating can then be analyzed, making possible the mapping of the gene(s) responsible for the trait with respect to the DNA marker loci, without requiring direct access to a specified gene's DNA. For inherited diseases mapped in this way, linked DNA marker loci can be used predictively for genetic counseling.
基于SSR标记的255个枣品种亲缘关系和群体遗传结构分析
DOI:10.3864/j.issn.0578-1752.2016.14.011
[本文引用: 1]

【目的】枣原产中国,种质资源丰富。对来自中国22个省区不同用途的255个枣品种进行SSR分析,揭示这些不同产地来源的枣种质资源之间的亲缘关系和群体遗传结构,为枣种质资源的科学管理和分子标记辅助育种提供参考。【方法】利用改良CTAB提取供试枣种质的基因组DNA,以前期枣基因组测序挖掘出的SSR引物为基础,进行高效率引物筛选,并利用SSR分子标记技术对255份枣种质资源的基因组DNA进行PCR扩增,然后利用8%聚丙烯酰胺凝胶电泳分离,银染后显色。根据条带有无统计数据,计算出多态性位点百分率(PIC),用NTSYS软件进行UPGMA聚类分析;利用Structure软件分析群体遗传结构,计算出最适群体数目,构建遗传结构图。【结果】从64对SSR引物中筛选出23对高效率SSR引物,在供试材料中共检测出117个多态性位点,各引物扩增的多态性位点数为2—10条,每对引物平均扩增多态位点数为5.09个,PIC值变幅为0.359—0.727,平均为0.548,这些多态性引物可应用到其他枣种质资源的研究中;建立了只需1—2个标记就可鉴别出来的部分枣品种的SSR指纹,可用于这些品种的快速分子鉴定;255个枣品种的聚类分析将所有枣品种分为15个亚类,包括4个大类和11个小类,不同品种间的相似系数范围0.71—1.00,其中北京花生枣单独聚为一类,与其他枣品种关系较远;‘奉节鸡蛋枣’和‘溆浦鸡蛋枣’、‘陕西奶枣’和‘天津大马牙枣’的相似系数均为1.00;结合聚类图、供试品种的用途和原产地分析,不同枣品种间的亲缘关系与品种原产地有一定相关性,但和品种用途没有显著相关性。群体结构分析中,通过绘制K与ΔK的关系图,K=15时,ΔK最大,据此将255个枣品种也同样划分为15个群体,与聚类分析结果基本一致;进一步分析表明,各群体中大部分品种血缘关系比较单一,较少品种含有其他类群的遗传成分。总体看,山西或陕西的枣品种出现在绝大部分居群中,说明这两个省的资源在不同群体间的基因交流中发挥了重要作用;南方栽培区域中来自湖南的枣品种形成了相对独立的居群,可能是其起源相对单一,且在长期栽培过程中和其他产地枣品种间基因交流较少所致。上述结果表明,供试枣品种中与来源区域相关性明显的品种由相同地域内枣品种演化而来,而另一部分与来源产地相关性不明显的品种则是由不同区域间品种经过频繁的基因交流和重组选育而来,融合了不同区域品种的特点,从而没有了明显的区域特征。【结论】不同地理环境在枣品种的群体进化中发挥了较重要的作用,影响了不同产地间枣种质资源的遗传结构组成。