茄子(Solanum melongena L.)是茄科中十分重要的蔬菜,具有较高的营养价值和药用价值。随着我国茄果类蔬菜集约式生产和保护地栽培面积的日益扩大,茄子土传病害呈逐渐加重的趋势[1]。研究[2]表明,嫁接可以增强植物抗性,对大部分病害有很好的防治作用。而嫁接砧木的缺乏影响了茄果类嫁接技术效益的发挥,所以优良砧木的选择变得至关重要。蔡鹏等[3]以野茄托鲁巴姆为砧木,发现嫁接后植株在生长势、坐果能力以及果实的商品性等方面都得到了明显的改善。潜宗伟等[4]用番茄作为砧木进行嫁接,发现其嫁接亲和力相对较低,表现为嫁接植株生长势降低及叶片数减少。因此,嫁接之后茄子植株性状能否得到提升与嫁接砧木的选择以及嫁接砧木和接穗之间的亲和性息息相关。多个研究[5-
目前,有关茄子嫁接方面的研究[8
1 材料与方法
1.1 试验材料
试验材料为水茄(StS)和云茄9号(Sm),其中水茄为云南省农业科学院园艺作物研究所茄子育种课题组收集、保存的云南野生茄资源,云茄9号则为课题组自育的茄子品种。
1.2 试验设计
1.2.1 砧木与接穗种子处理及嫁接苗培养
将水茄(由于水茄发芽相对困难,所以需要提前15~20 d完成播种)与云茄9号种子分别置于40目的尼龙种子袋,在55 ℃的水浴锅中消毒15 min,之后用无菌水清洗2~3次,在25 ℃温水下浸种6~8 h。再用浓度为400 mg/L的赤霉素(GA3)溶液浸泡24 h,浸泡后置于28~30 ℃恒温培养箱中,每天用清水淘洗2次,待85%左右的种子露白后即可播种。用穴盘(长54 cm、宽28 cm,5×10排列)进行育苗,每穴挑选3粒发芽程度一致的种子进行播种。播种后,温度控制在28~30 ℃,湿度保持在60%~70%。
1.2.2 砧木与接穗苗的嫁接
选取生长健康、粗度相近的植株进行嫁接,如图1所示。待砧木粗度达3~4 mm,长有5~7片真叶,接穗达4~6片真叶时进行劈接。嫁接前将刀片和嫁接夹用75%酒精浸泡消毒。用刀片从砧木根部往上5 cm处将其上部茎叶削去,再沿切面中心向下纵切1 cm左右;在接穗顶部2~3片真叶下方1.5 cm处水平切断,在其基部沿切口处削成长约1 cm左右的楔形,迅速插入砧木切口中,立即用嫁接夹固定好接口处。
图1
图1
水茄和云茄9号嫁接苗
(a) 水茄自体嫁接苗(StS/StS);(b) 云茄9号自体嫁接苗(Sm/Sm);(c) 以水茄为砧木、云茄9号为接穗的嫁接苗(Sm/StS)。
Fig.1
The grafting of S. torvum Swartz. and S. melongena Yunqie 9
(a) self grafting seedlings of S. torvum Swartz. (StS/StS); (b) self grafting seedlings of S. melongena Yunqie 9 (Sm/Sm); (c) grafting seedlings using S. torvum Swartz. as rootstock and S. melongena ʻYunqie 9ʼ as scion (Sm/StS).
1.2.3 嫁接苗管理
嫁接后早晚盖塑料薄膜保湿,前3 d置于阴凉处,中午通风,白天温度控制在25~ 28 ℃,夜晚控制在15~18 ℃,保持空气湿度为95%,5~7 d后正常管理。
1.2.4 组织切片材料取样
设3个处理:水茄自体嫁接苗(StS/StS)、云茄9号自体嫁接苗(Sm/Sm),以及以水茄为砧木、云茄9号为接穗的嫁接苗(Sm/StS),分别于嫁接后12 d内每2 d取样1次,共取样7次(即嫁接后0、2、4、6、8、10和12 d)。每次分别随机选取长势相近的健壮苗处理组(Sm/StS)与对照组(StS/StS、Sm/Sm)各5株,切取砧穗结合部茎段(1~1.5 cm)以及从上往下的第3~4片真叶,茎段用于制作石蜡切片,叶片用于生理测定。
1.3 试验方法
1.3.1 材料的软化与固定
将1.2.4中所取茎段用封口膜固定好,放入由95% FAA固定液和5%甘油组成的混合液中常温固定3~5 d,将固定好的样品放入植物组织软化液中软化15 d。
1.3.2 石蜡切片的制作
(1)脱水:75%乙醇40 min →85%乙醇40 min→90%乙醇40 min→95%乙醇40 min→无水乙醇I 40 min→无水乙醇Ⅱ 40 min。
(2)透明:50%乙醇+50%二甲苯25 min→二甲苯Ⅰ 30 min→二甲苯Ⅱ 25 min。
(3)浸蜡:将透明好的组织块置入已熔化的58~60 ℃石蜡内,共3杯蜡,第1杯蜡40 min,第2杯蜡60 min,第3杯90 min,使之逐步排出组织中的透明剂二甲苯,让石蜡易于渗入。
(4)包埋:将过滤好的新蜡倾入HistoCore ArCadia H包埋器(徕卡,德国)中,尽快将浸透蜡的组织块放到里面。将组织块的切面朝下,组织与蜡之间不能留有空隙,力求摆正摆平,尽量与包埋器底板接触,最后放上标纸。
(5)连续切片:用HistoCore BloCu7石蜡切片机(徕卡,德国)将石蜡块切成4 µm厚的切片。
(6)贴片:切好的石蜡组织片先放入冷水中进行第1次展片,再转入45 ℃的温水中进行第2次展片,最后再用经过多聚赖氨酸包被处理的载玻片将组织切片捞起并贴附于载玻片上。
(7)烤片:将贴有石蜡切片的载玻片放置于载玻片架上,在60 ℃烤箱烘烤1~2 h。
1.3.3 番红固绿染色与观察
(1)将石蜡切片进行常规脱蜡、水化:60 ℃烘片30 min→二甲苯I 10 min→二甲苯Ⅱ 10 min→二甲苯III 10 min→无水乙醇I 5 min→无水乙醇II 5 min→95%乙醇5 min→90%乙醇5 min→80%乙醇5 min→70%乙醇5 min→蒸馏水I 5 min→蒸馏水Ⅱ 5 min。(2)番红染液染5 min。(3)50%酒精分化5~30 s,75%酒精分化5~30 s。(4)固绿染液染色30~60 s。(5)无水脱水5~30 s,二甲苯透明5~30 s。(6)中性树胶封片。(7)用数字切片扫描仪进行全息扫描(3DHISTECH,Pannoramic MIDI)。
1.4 测定项目与方法
将1.2.4中所取叶片剪碎混匀后,按0.2 g/管分装于试管中,每个样品设置3个生物学重复,并按过氧化物酶(POD,A084-3-1)、苯丙氨酸解氨酶(PAL,A137-1-1)、超氧化物歧化酶(SOD,A001-1)以及可溶性蛋白(SP,A045-2)试剂盒进行测定,所有试剂盒均购自南京建成生物科技有限公司,具体酶活性测定与计算方法按对应说明书进行。
1.5 数据处理
利用软件Excel 2021处理数据,利用软件SPSS 26.0进行显著性分析,采用Duncan法进行多重比较,利用软件Origin 2021进行图表绘制。
2 结果与分析
2.1 愈伤组织石蜡切片的观察
2.1.1 隔离层与愈伤组织形成期
图2
图2
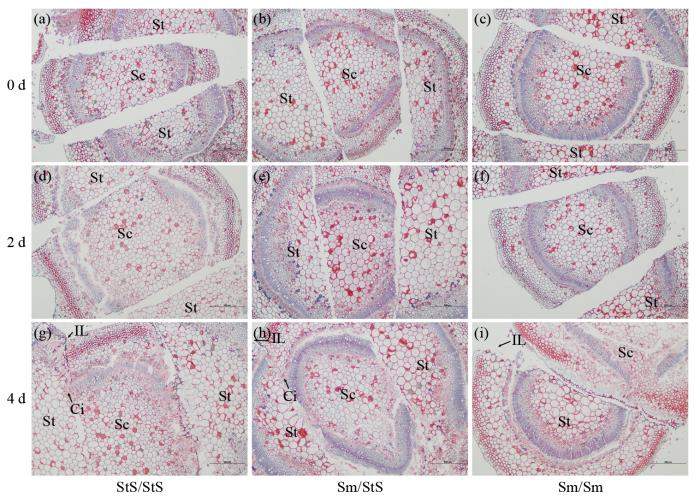
嫁接后0、2和4 d砧穗结合部横切面显微结构
St:砧木;Sc:接穗;IL:隔离层;Ci:愈伤组织,刻度标尺为500 μm,下同。
Fig.2
The cross sectional microstructure of graft union at 0, 2 and 4 days after grafting
St: rootstock; Sc: scion; IL: isolation layer; Ci: callus tissue, the scale is 500 μm, the same below.
2.1.2 愈伤组织分裂与增殖连接期
图3
图3
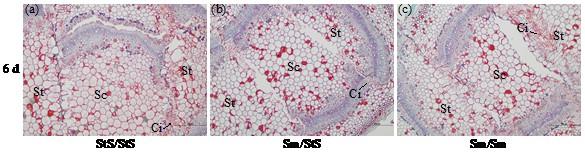
嫁接后6 d砧穗结合部横切面显微结构
Fig.3
The cross sectional microstructure of graft union at 6 days after grafting
2.1.3 形成层连接期
图4
图4
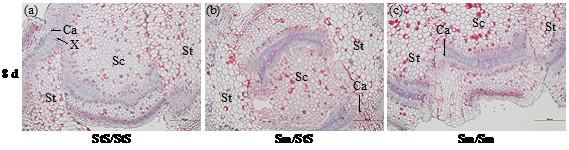
嫁接后8 d砧穗结合部显微结构
Ca:形成层,下同。
Fig.4
The cross sectional microstructure of graft union at 8 days after grafting
Ca: cambium, the same below.
2.1.4 维管组织分化形成期
图5
图5
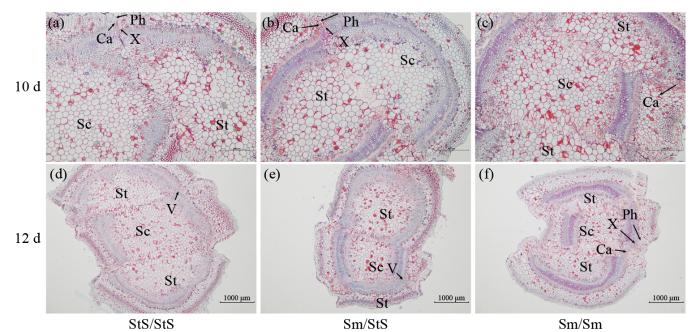
嫁接后10和12 d砧穗结合部横切面显微结构
Ph:韧皮部;X:木质部;V:导管。
Fig.5
The cross sectional microstructure of graft union at 10 and 12 days after grafting
Ph: phloem; X: xylem; V: vessel.
2.2 嫁接愈合过程中的生理变化
2.2.1 苯丙氨酸解氨酶(PAL)活性变化
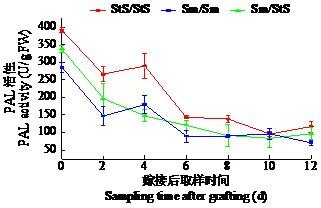
由图6可知,在嫁接愈合过程中,嫁接苗Sm/StS、StS/StS和Sm/Sm在嫁接后0~2 d的PAL活性变化趋势一致,PAL活性极速下降,此时Sm/StS的PAL活性介于StS/StS和Sm/Sm之间。而嫁接后2~4 d时,StS/StS、Sm/Sm和Sm/StS嫁接苗嫁接部位出现差异,自体嫁接苗PAL活性逐渐上升,而Sm/StS的PAL活性仍处于下降趋势,持续到10 d时开始上升。Sm/StS的PAL活性在前10 d总体处于下降趋势,在10 d时出现拐点,同时也是其最低值,为84.05 U/g,而StS/StS和Sm/StS在6 d之后变化趋势一致,与Sm/Sm变化趋势相反。
图6
图6
水茄和云茄9号嫁接愈合过程中PAL活性变化
Fig.6
Changes in PAL activity during the healing process of S. torvum Swartz. and S. melongena Yunqie 9 grafting
2.2.2 超氧化物歧化酶(SOD)活性变化
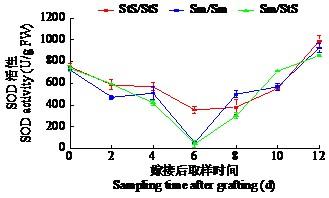
由图7可知,Sm/StS与StS/StS和Sm/Sm的SOD活性总体变化趋势均呈现“V”形,除嫁接后2~4 d外,三者整体变化趋势一致,均在6 d时出现最低值。Sm/StS在0~6 d过程中SOD活性明显下降,于6 d时达到最低值(43.55 U/g),后又于6~12 d时显著上升达到最高值(858.72 U/g),最高值与最低值相差19倍,与StS/StS和Sm/Sm相比,Sm/StS在2~4 d下降趋势更明显。
图7
图7
水茄和云茄9号嫁接愈合过程中SOD活性变化
Fig.7
Changes in SOD activity during the healing process of S. torvum Swartz. and S. melongena Yunqie 9 grafting
2.2.3 过氧化物酶(POD)活性变化
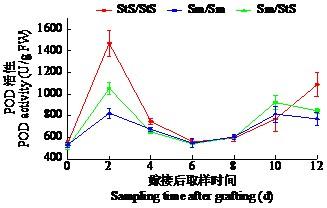
如图8所示,Sm/StS与StS/StS、Sm/Sm前0~10 d整体变化趋势一致,在10~12 d时,StS/StS的POD活性大幅度上升,而Sm/StS和Sm/Sm处于下降趋势。相对于自体嫁接苗,Sm/StS的POD活性总体变化趋势比较平稳。出现变化的主要时间节点为2、6和10 d。
图8
图8
水茄和云茄9号嫁接愈合过程中POD活性变化
Fig.8
Changes in POD activity during the healing process of S. torvum Swartz. and S. melongena Yunqie 9 grafting
2.2.4 可溶性蛋白(SP)含量变化
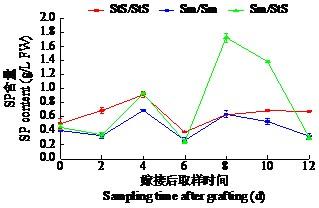
如图9所示,Sm/StS与StS/StS、Sm/Sm可溶性蛋白含量变化趋势整体呈现“M”形,且Sm/StS变化比较剧烈,主要拐点出现在2、4、6和8 d,其中最低点为6 d(0.30 g/L),最高点为8 d(1.73 g/L),两者相差5.6倍。Sm/StS的SP含量在0~6 d时位于StS/StS和Sm/Sm之间,而6~8 d时急剧上升,明显高于自体嫁接苗。与StS/StS和Sm/Sm相比,嫁接苗Sm/StS在8 d时的SP含量变化明显,是两者的2.7倍,说明SP的含量受嫁接的影响作用比较明显。
图9
图9
水茄和云茄9号嫁接愈合过程中SP含量变化
Fig.9
Changes in SP content during the healing process of S. torvum Swartz. and S. melongena Yunqie 9 grafting
3 讨论
嫁接可以结合砧木和接穗的优良特性,增强植物的抗病抗虫能力,是一种极为重要的无性繁殖方法[12]。而嫁接植物能否按照人们的预期行使正常的生物功能,愈合过程十分关键,圆齿野鸦椿[13]嫁接愈合过程可分为3个时期,山苍子[14]的嫁接愈合过程可分为4个时期,千年桐[15]嫁接愈合过程可分为5个时期。虽然不同物种嫁接愈合进程存在差异,但基本的愈合过程大致相似,本研究发现水茄与云茄9号嫁接愈合过程可分为4个主要时期:隔离层与愈伤组织形成期(0~4 d)、愈伤组织分裂与增殖连接期(5~7 d)、形成层连接期(8~9 d)和维管组织分化形成期(10~12 d)。由此可见,嫁接愈合时期的确定主要是根据砧穗间的愈合情况而定,而砧穗间的快速愈合会受到许多因素的影响。
隔离层的形成可以减少外界不利因素对嫁接部位带来的伤害,本研究与祁利潘等[16]在马铃薯与枸杞嫁接愈合过程的研究不同,嫁接苗在4 d就形成了对伤口有保护作用的隔离层,产生这种差异的原因可能是不同物种间亲和性不同所导致。愈伤组织桥的形成构建了接穗与砧木之间的水分及养料交流的通道,是嫁接愈合的关键一环。水茄与云茄9号嫁接后6 d,嫁接部位愈伤组织开始大量分裂增殖并逐步连接在一起形成了愈伤组织桥,这与解华云等[17]在薄皮甜瓜嫁接砧穗愈合过程组织学观察的研究结果相似。形成层恢复是嫁接成功的标志性事件之一,水茄与云茄9号嫁接后8 d时嫁接苗砧穗位置不仅形成层连接在一起,而且形成层处已经开始有向内分化出木质部、向外分化出韧皮部的趋势。而维管束重新连接标志着嫁接成功[18],嫁接后10 d,嫁接结合部形成层连接处能明显看到分化出了象征嫁接成活的维管组织并且形成层处已开始向内分化出木质部,向外分化出韧皮部,当嫁接苗于12 d时在嫁接结合部位形成了新的导管且木质部和韧皮部分化更加明显,此时嫁接苗已经完全愈合为一个新的个体。
PAL是嫁接愈合过程中新个体功能重建及组织发育的重要因子,具有促进细胞分化及木质化的功能[21]。在本研究中,自体嫁接苗和嫁接苗在嫁接初期变化趋势一致,而6 d之后水茄自体嫁接苗与水茄为砧木、云茄9号为接穗的嫁接苗和云茄9号自嫁接苗变化趋势相反,说明嫁接愈合过程中嫁接苗受水茄的影响较大,而前期嫁接苗PAL变化一直呈下降趋势,表明了嫁接愈合速度的快慢与嫁接亲和性息息相关,自体嫁接苗的愈合速度显著高于嫁接苗愈合速度,出现这种差异的原因可能是创伤口与嫁接口的木质化程度不同所致。到10 d时嫁接苗PAL活性开始上升,此时细胞分化和木质化速度加快,与切片维管组织分化形成期组织结构变化相吻合。
砧木和接穗之间的相容性很大程度上取决于愈合处愈伤组织细胞的形成,而愈伤组织又受特定蛋白质的控制,SP在维持嫁接苗的生长和代谢中起到了重要的作用[24]。本次嫁接过程中,嫁接苗SP含量在2~4 d时上升,在细胞学上对应隔离层与愈伤组织形成期,可以有效减少细胞失水并保护细胞生物膜,而8~12 d时急速下降,此时处于形成层连接期和维管组织分化形成期,是嫁接体愈合的关键阶段,需要消耗大量蛋白质用于合成细胞结构和提供能量,从而推进机体分裂和分化快速进行。
4 结论
通过石蜡切片技术对水茄与云茄9号嫁接结合部不同时间点的组织结构观察发现,其愈合过程可分为4个主要时期。根据生理结果可知,PAL活性变化的主要时间点为嫁接后2、4、8和10 d,SOD活性变化的主要时间点为嫁接后4和6 d,POD活性变化的主要时间点为嫁接后2、6、8和10 d,SP含量变化的主要时间点为嫁接后2、4、6和8 d。综上所述,水茄与云茄9号嫁接后4、6和8 d很可能是其关键愈合时间点。
参考文献
Plant grafting: molecular mechanisms and applications
DOI:10.1016/j.molp.2023.12.006 URL [本文引用: 1]
茄子嫁接栽培防治根结线虫砧木的筛选
嫁接方法对茄子嫁接工效、嫁接苗生长发育的影响
嫁接对茄子栽培及田间抗逆性影响的研究
千年桐嫁接愈合过程解剖结构与内源激素的变化
为探索千年桐(Vernicia montana)嫁接愈合机理,以千年桐嫁接口茎段为试材,采用硬组织切片法,观察嫁接愈合进程中的组织结构;采用酶联免疫吸附法测定结合部形成层及韧皮部相关内源激素含量。结果表明,嫁接后第5天,接口处出现隔离层;嫁接后第7天,愈伤组织形成;嫁接后第11天,形成愈伤组织桥;嫁接后第17天,形成形成层;嫁接后第25天,形成层向内分生出木质部。IAA含量在嫁接后第13、17、25、34和43天处于峰值,在嫁接后第17天最高;ABA含量在嫁接后第11、25、34和43天处于峰值;GA<sub>3</sub>含量在嫁接后第11、17、22、34和46天处于峰值;ZR含量在嫁接后第9、13、25和43天处于峰值。IAA、ABA、GA<sub>3</sub>和ZR的含量在嫁接后第7、19、28和37天处于谷值,IAA、ABA和GA<sub>3</sub>的含量均在嫁接后第28天的值最低。愈合过程历经隔离层期(第1 ~ 5 天)、愈伤组织分化形成期(第5 ~ 9 天)、愈伤组织连接期(第9 ~ 17天)、形成层分化连接期(第17 ~ 25 天)和维管组织分化连接期(第25 ~ 34天)。嫁接后前9天是决定嫁接体能否形成的关键期,前34天是嫁接苗成活的重要时期。
马铃薯与枸杞嫁接愈合过程的解剖学观察
DOI:10.16420/j.issn.0513-353x.2021-0198
[本文引用: 1]

为揭示马铃薯与枸杞嫁接愈合过程,采用石蜡切片技术对马铃薯/枸杞嫁接植株进行解剖学观察。结果显示:马铃薯/枸杞嫁接植株生长旺盛,可完成整个生育进程。马铃薯/枸杞嫁接愈合过程可分为4个阶段:(1)隔离层产生期,嫁接5 d后,嫁接接口处产生隔离层;(2)愈伤组织形成期,嫁接9 d后,隔离层细胞脱分化,最后形成愈伤组织;(3)愈伤组织分化期,嫁接13 d后,愈伤组织分化,形成愈伤组织桥;(4)新的维管组织形成期,嫁接17 d后,形成新的韧皮部和木质部及维管束桥,使砧木和接穗完全结合,愈合过程结束。
Plant grafting
DOI:10.1016/j.cub.2015.01.029
PMID:25734263
[本文引用: 1]

Since ancient times, people have cut and joined together plants of different varieties or species so they would grow as a single plant - a process known as grafting (Figures 1 and 2). References to grafting appear in the Bible, ancient Greek and ancient Chinese texts, indicating that grafting was practised in Europe, the Middle East and Asia by at least the 5(th) century BCE. It is unknown where or how grafting was first discovered, but it is likely that natural grafting, the process by which two plants touch and fuse limbs or roots in the absence of human interference (Figure 3), influenced people's thinking. Such natural grafts are generally uncommon, but are seen in certain species, including English ivy. Parasitic plants, such as mistletoe, that grow and feed on often unrelated species may have also contributed to the development of grafting as a technique, as people would have observed mistletoe growing on trees such as apples or poplars. Copyright © 2015 Elsevier Ltd. All rights reserved.
An insight into dwarfing mechanism: contribution of scion-rootstock interactions toward fruit crop improvement
Effect of salinity on growth, mineral composition, and water relations of grafted tomato plants
DOI:10.1002/jpln.v167:5 URL [本文引用: 1]