作物杂志,2018, 第1期: 56–61 doi: 10.16035/j.issn.1001-7283.2018.01.008
农杆菌介导高粱遗传转化的相关因素优化
张微1,2,王良群1,2,刘勇1,郝艳芳1,2,杨伟1,白鸿雁1,武擘1
- 1 高粱遗传与种质创新山西省重点实验室,030600,山西晋中
2 山西省农业科学院高粱研究所,030600,山西晋中
Optimization of the Factors Related to the Efficiency of Agrobacterium-Mediated Transformation of Sorghum
Zhang Wei1,2,Wang Liangqun1,2,Liu Yong1,Hao Yanfang1,2,Yang Wei1,Bai Hongyan1,Wu Bo1
- 1 Shanxi Key Laboratory of Sorghum Genetic and Germplasm Innovation, Jinzhong 030600, Shanxi, China
2 Sorghum Institute, Shanxi Academy of Agricultural Sciences, Jinzhong 030600, Shanxi, China
摘要:
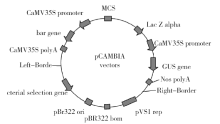
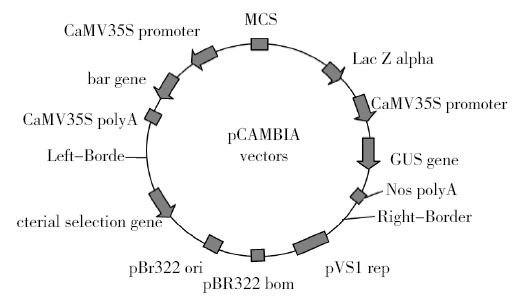
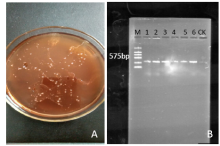
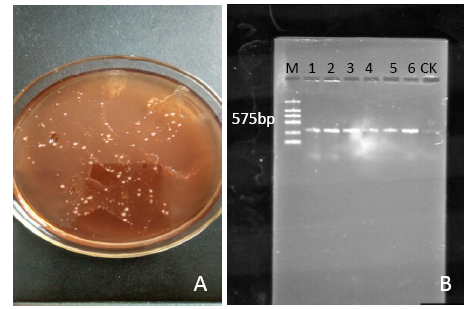
为建立一个稳定的高粱遗传转化体系,以高粱RHMC品种为试验材料,采用内含有P CAMBIA3301质粒载体的根癌农杆菌EHA105介导的方法研究了高粱遗传转化的相关因素。结果表明,外植体预培养2d,GUS表达效果最好;在侵染液和共培养基中加入200μmol/L乙酰丁香酮时,GUS表达效果最好;侵染液浓度OD600值的适宜范围为0.8~1.0;农杆菌侵染愈伤组织的适宜时间为5~10min;共培养的适宜时间为2d。初步建立了一套高粱遗传转化体系,为今后高粱转化提供一些参考。
| [1] | Saballos A . Development and utilization of sorghum as a bioenergy. In:Vermerris W. Genetic Improvement of Bioenergy Crops. New York:Springer, 2008: 211-248. |
| [2] | Liang G H, Gao Z S . Phylogenetic analysis and transformation of sorghum [Sorghum bicolor (L.) Moench]. Recent Research Developmental Biology, 2001,1:17-33. |
| [3] |
Anshu R, Robert G, Birch . Genetic transformation of sweet sorghum, Plant Cell Reports, 2010,29:997-1005.
doi: 10.1007/s00299-010-0885-x pmid: 20535472 |
| [4] |
Rooney W L, Blumenthal J, Bean B , et al. Designing sorghum as a dedicated bioenergy feedstock. Biofuels Bioproducts and Bioproducts, 2007,1:147-157.
doi: 10.1002/bbb.15 |
| [5] | 张微, 王良群, 刘勇 , 等. 高粱遗传转化研究进展. 安徽农业科学, 2015,43(27):387-389. |
| [6] | 魏开发, 刘逸萍, 林子英 , 等. 农杆菌介导单子叶植物遗传转化问题与对策. 植物学通报, 2008,25(4):491-496. |
| [7] | 周逢勇, 王国英 . 玉米自交系P9-10遗传转化体系的建立. 科学通报, 1988(23):2517-2520. |
| [8] | 黄璐, 卫志明 . 农杆菌介导的玉米遗传转化. 实验生物学报, 1999,32(4):381-387. |
| [9] | 刘明志 . 论农杆菌介导的单子叶植物转化. 遗传, 1996(增刊):50-52. |
| [10] |
Suncan D R . The production of callus capable of plant regeneration from immature embryos of numerous Zea mays genotypes. Planta, 1985,165:322-332.
doi: 10.1007/BF00392228 |
| [11] | Zhu H, Muthukrishnan S, Krishnaveni S , et al. Biolistic transformation of sorghum using a rice chitinase gene. Journal of Genetics & Breeding, 1998,52:243-252. |
| [12] |
朱莉, 郎志宏, 李桂英 , 等. 高粱遗传转化研究进展. 生物技术通报, 2011(1):1-7,113.
doi: 10.3724/SP.J.1259.2011.00216 |
| [13] |
Lu L, Wu X R, Yin X Y , et al. Development of marker-free trans genic sorghum [Sorghum bicolor (L.) Moench] using standard binary vectors with barasa selectable emarker. Plant Cell, Tissue and Organ Culture, 2009,99(1):97-108.
doi: 10.1007/s11240-009-9580-4 |
| [14] |
付超, 王婷婷, 银利辉 , 等. 农杆菌介导番茄遗传转化的相关因素优化. 分子植物育种, 2013,11(5):592-599.
doi: 10.3969/mpb.011.000592 |
| [15] |
林凤, 石太渊, 赵淑华 , 等. 根癌农杆菌介导的高粱遗传转化体系的研究. 生物技术, 2004,14(1):13-14.
doi: 10.3969/j.issn.1004-311X.2004.01.006 |
| [16] |
朱莉, 郎志宏, 李桂英 , 等. 农杆菌介导甜高粱转Btcry1Ah的研究. 中国农业科学, 2011,44(10):1989-1996.
doi: 10.3864/j.issn.0578-1752.2011.10.003 |
| [17] |
肖军, 石太渊, 王金艳 . 高粱遗传转化研究进展. 辽宁农业科学, 2003(5):38-40.
doi: 10.3969/j.issn.1002-1728.2003.05.014 |
| [18] |
Zhao Z Y, Cai T, Taglini L , et al. Agrobacterium-mediated sorghum transformation. Plant Molecular Biology, 2000,44:789-798.
doi: 10.1023/A:1026507517182 |
| [19] |
肖军, 石太渊, 郑秀春 , 等. 根癌农杆菌介导的高粱遗传转化体系的建立. 杂粮作物, 2004,24(4):200-203.
doi: 10.3969/j.issn.2095-0896.2004.04.006 |
| [20] |
张明洲, 唐乔, 陈宗伦 , 等. 农杆菌介导Bt基因遗传转化高粱. 生物工程学报, 2009,25(3):418-423.
doi: 10.3321/j.issn:1000-3061.2009.03.016 |
| [21] | 张明洲, 陈宗伦, 方美明 , 等. 转基因高粱Cry1Ab蛋白含量的比较研究. 核农学报, 2009,23(3):391-394. |
| [22] | 吴仙花 . 农杆菌介导甜高粱Bar基因再生体系建立及水稻EIS基因转化研究. 天津:天津农学院, 2014. |
| [1] | 张一中, 周福平 张晓娟 邵 强 杨 彬 柳青山. 高粱种质材料光合特性和水分#br# 利用效率鉴定及聚类分析[J]. 作物杂志, 2018, (5): 45–53 |
| [2] | 张瑞栋 曹 雄 岳忠孝 梁晓红 刘 静 黄敏佳. 氮肥和密度对高粱产量及氮肥利用率的影响[J]. 作物杂志, 2018, (5): 110–115 |
| [3] | 张建华 郭瑞峰 曹昌林 范 娜 江佰阳. 几种茎叶除草剂防除高粱田杂草药效和安全性研究[J]. 作物杂志, 2018, (5): 162–166 |
| [4] | 高杰,李青风,彭秋,焦晓燕,王劲松. 不同养分配比对糯高粱物质生产及氮磷钾利用效率的影响[J]. 作物杂志, 2018, (4): 138–142 |
| [5] | 张姣,吴奇,周宇飞,王艺陶,张瑞栋,黄瑞冬. 苗期和灌浆期干旱-复水对高粱光合特性和物质生产的影响[J]. 作物杂志, 2018, (3): 148–154 |
| [6] | 崔江辉,崔福柱,薛建福,郝建平,杜天庆,孙隆祥. 化肥减施对小麦-高粱系统土壤团聚体分布及其稳定性的影响[J]. 作物杂志, 2018, (1): 126–132 |
| [7] | 郝艳芳,王良群,刘勇,张微,杨伟,白鸿雁,武擘. 高粱幼叶细胞悬浮系的建立[J]. 作物杂志, 2018, (1): 35–40 |
| [8] | 朱凯,张飞,柯福来,王艳秋,邹剑秋. 种植密度对适宜机械化栽培高粱品种产量及生理特性的影响[J]. 作物杂志, 2018, (1): 83–87 |
| [9] | 高杰,李青风,汪灿,张国兵,彭秋. 不同氮素水平对糯高粱物质生产及氮素利用特性的影响[J]. 作物杂志, 2017, (6): 126–130 |
| [10] | 王聪,杨广东,胡尊艳,陈林祺,任思琪. 种植密度对高粱冠层结构及光辐射特征的影响[J]. 作物杂志, 2017, (5): 119–123 |
| [11] | 丁超,张建华,白文斌,郭瑞峰,曹昌林. 高粱田常用除草剂对高粱生理生化及产量品质的影响[J]. 作物杂志, 2017, (5): 149–155 |
| [12] | 于纪珍,王瑞,詹鹏杰,平俊爱,张福耀. 中国主要高粱杂交种农艺及品质性状多样性分析[J]. 作物杂志, 2017, (5): 49–54 |
| [13] | 张伟,张阳,赵威军,邵荣峰,卜华虎,常玉卉,李金梅,王花云. 烯效唑对甜高粱农艺性状及倒伏率的影响[J]. 作物杂志, 2017, (4): 113–116 |
| [14] | 张晓娟,周福平,张一中,邵强,范昕琦,刘勇,柳青山. 复粒高粱不育系的研究[J]. 作物杂志, 2017, (2): 72–75 |
| [15] | 王欢,刘冰,白子裕,史俊丽,叶锦琳. 激光辐射和杂交对高粱DNA甲基化变异的影响[J]. 作物杂志, 2017, (1): 32–37 |
|