作物杂志,2023, 第4期: 230–236 doi: 10.16035/j.issn.1001-7283.2023.04.033
所属专题: 杂粮作物
氟磺胺草醚胁迫红小豆幼苗代谢物及通路分析
杨建1,2( ), 汤华成1,2,3,4(
), 汤华成1,2,3,4( ), 曹冬梅1,2,3,4(
), 曹冬梅1,2,3,4( ), 崔航1,2, 娄雨豪1,2, 王冀菲1,2, 张东杰1,3,5
), 崔航1,2, 娄雨豪1,2, 王冀菲1,2, 张东杰1,3,5
- 1黑龙江八一农垦大学食品学院,163319,黑龙江大庆
2黑龙江省农产品加工与质量安全重点实验室,163319,黑龙江大庆
3黑龙江省杂粮加工及质量安全工程技术研究中心,163319,黑龙江大庆
4国家杂粮工程技术研究中心,163319,黑龙江大庆
5北大荒现代农业产业技术省级培育协同创新中心,163319,黑龙江大庆
Analysis of Metabolites and Pathways in Adzuki Bean Seedlings under Fomesafen Stress
Yang Jian1,2( ), Tang Huacheng1,2,3,4(
), Tang Huacheng1,2,3,4( ), Cao Dongmei1,2,3,4(
), Cao Dongmei1,2,3,4( ), Cui Hang1,2, Lou Yuhao1,2, Wang Jifei1,2, Zhang Dongjie1,3,5
), Cui Hang1,2, Lou Yuhao1,2, Wang Jifei1,2, Zhang Dongjie1,3,5
- 1College of Food Science, Heilongjiang Bayi Agricultural University, Daqing 163319, Heilongjiang, China
2Key Laboratory of Agro-Products Processing and Quality Safety of Heilongjiang Province, Daqing 163319, Heilongjiang, China
3Heilongjiang Engineering Research Center for Coarse Cereals Processing and Quality Safety, Daqing 163319, Heilongjiang, China
4National Coarse Grain Engineering Research Center, Daqing 163319, Heilongjiang, China
5Beidahuang Modern Agricultural Industrial Technology Provincial Cultivation Collaborative Innovation Center, Daqing 163319, Heilongjiang, China
摘要:
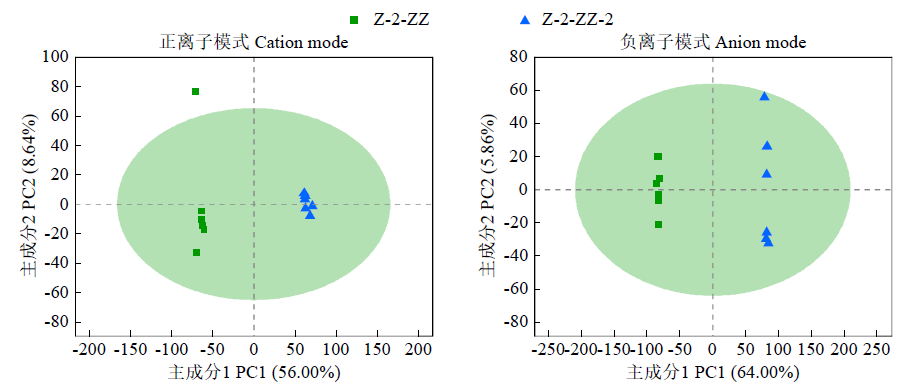
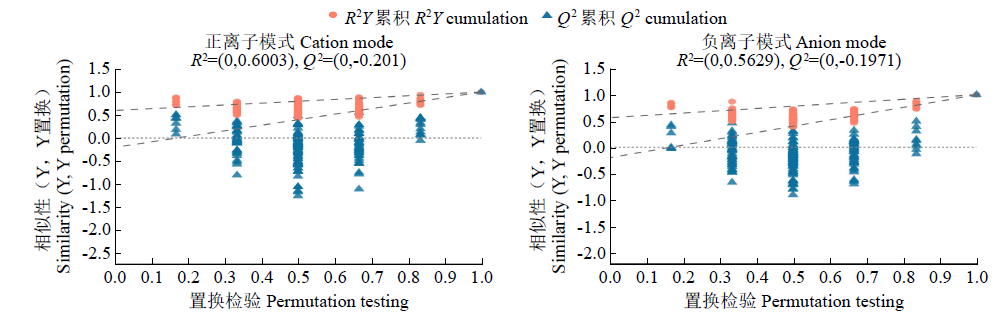
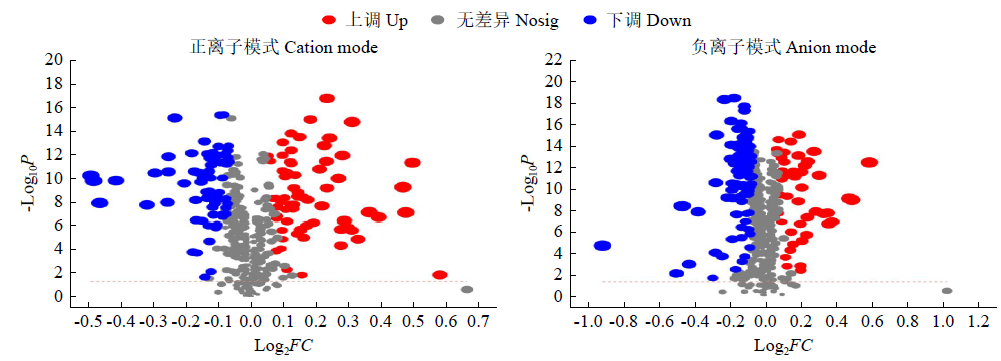
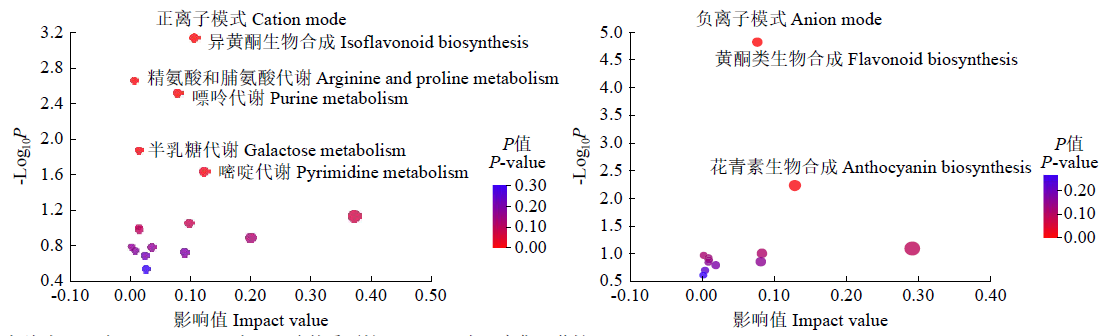
为探究田间喷施氟磺胺草醚(FSA)对红小豆幼苗生长代谢的调控机制,以是否喷施FSA的红小豆幼苗为试验材料,采用液相色谱-质谱联用(LC-MS)代谢组学技术对红小豆幼苗代谢物的变化进行分析。结果表明,喷药的红小豆幼苗(Z-2-ZZ-2)组与未喷药红小豆幼苗(Z-2-ZZ)组相比,正离子模式下筛选出显著变化的差异代谢物106种(上调50种,下调56种),负离子模式下130种(上调42种,下调88种),正离子模式下注释到差异显著的代谢通路5条(嘧啶代谢、异黄酮生物合成、嘌呤代谢、半乳糖代谢、精氨酸和脯氨酸代谢),映射到差异代谢物13种,负离子模式下注释到差异显著的代谢通路2条(花青素生物合成和黄酮类生物合成),映射到差异代谢物5种。苯丙烷和聚酮化合物、脂质、类脂分子、有机酸及其衍生物类化合物在红小豆幼苗抵御FSA的胁迫中起主要作用。本研究为红小豆田间使用FSA的安全性评价及红小豆增收增产提供新思路。
| [1] |
张波, 薛文通. 红小豆功能特性研究进展. 食品科学, 2012, 33(9):264-266.
doi: 10.7506/spkx1002-6630-201209055 |
| [2] | 陶波, 池源, 滕春红, 等. 助剂对氟磺胺草醚在土壤中分布影响研究. 东北农业大学学报, 2018, 49(4):21-28. |
| [3] | 陈未, 李江叶, 刘丽珠, 等. 氟磺胺草醚对不同豆科作物生长及根际固氮菌的影响. 农业环境科学学报, 2021, 40(10):2076-2085. |
| [4] | 季磊, 马晓健, 曲悠扬, 等. 高效液相色谱法测定甘草、黄芪和葛根中除草剂氟磺胺草醚和氯嘧磺隆的残留量. 农药科学与管理, 2020, 41(9):37-42. |
| [5] |
Wu X H, Zhang Y, Du P Q, et al. Impact of fomesafen on the soil microbial communities in soybean fields in Northeastern China. Ecotoxicology and Environmental Safety, 2017, 148(3):169-176.
doi: 10.1016/j.ecoenv.2017.10.003 |
| [6] | Li Z N, Gioia F D, Hwang J I, et al. Dissipation of fomesafen in fumigated, anaerobic soil disinfestation-treated, and organic- amended soil in Florida tomato production systems. Pest Management Science, 2020, 76(2):6-16. |
| [7] |
Meng L, Sun T, Li M, et al. Soil-applied biochar increases microbial diversity and wheat plant performance under herbicide fomesafen stress. Ecotoxicology and Environmental Safety, 2018, 171:75-83.
doi: 10.1016/j.ecoenv.2018.12.065 |
| [8] |
Reed T V, Boyd N S, Wilson P C, et al. Persistence and movement of fomesafen in Florida strawberry production. Weed Science, 2018, 66(6):773-779.
doi: 10.1017/wsc.2018.48 |
| [9] |
Khorram M S, Zheng Y, Lin D, et al. Dissipation of fomesafen in biochar-amended soil and its availability to corn (Zea mays L.) and earthworm (Eisenia fetida). Journal of Soils and Sediments, 2016, 16(10):2439-2448.
doi: 10.1007/s11368-016-1407-4 |
| [10] | 王法武, 杨微, 李洪鑫, 等. 氟磺胺草醚·烯草酮乳油对绿豆及红小豆田杂草药效试验. 东北农业科学, 2017, 42(4):30-32. |
| [11] | 黄春艳, 王宇, 黄元炬, 等. 8种除草剂对红小豆田杂草的防除效果及对红小豆的安全性. 杂草科学, 2014, 32(1):101-106. |
| [12] | 丁伟, 杨隆华, 程茁, 等. 氟磺胺草醚对大豆根瘤固氮酶活性及光合速率的影响. 作物杂志, 2010(4):81-84. |
| [13] | 纪广影, 丁伟, 高文逸, 等. 氟磺胺草醚抑制大豆根瘤固氮酶活性与碳代谢关系的研究. 江苏农业科学, 2018, 46(8):92-95. |
| [14] | 程茁, 杨隆华, 丁伟, 等. 氟磺胺草醚对大豆根瘤固氮和蔗糖代谢的影响. 作物杂志, 2011(6):24-27. |
| [15] |
Fiehn O. Metabolomics the link between genotypes and phenotypes. Plant Molecular Biology, 2002, 48(1):155-171.
doi: 10.1023/A:1013713905833 |
| [16] |
雷刚, 黄英金. 代谢组学在水稻研究中的应用进展. 中国农业科技导报, 2017, 19(7):27-35.
doi: 10.13304/j.nykjdb.2017.0068 |
| [17] |
Feng Z, Sun X, Yang J, et al. Metabonomics analysis of urine and plasma from rats given long-term and low-dose dimethoate by ultra-performance liquid chromatography-mass spectrometry. Chemico-Biological Interactions, 2012, 199(3):143-153.
doi: 10.1016/j.cbi.2012.07.004 pmid: 22884955 |
| [18] | 庄明亮, 李志勇, 王进州, 等. 基于LC-MS技术的代谢组学方法研究吡虫啉对工蜂代谢的影响. 中国畜牧兽医, 2019, 46(8):2220-2227. |
| [19] | 蔡光辉. 代谢组学技术研究苯唑草酮对玉米幼苗代谢的影响. 新乡:河南科技学院, 2021. |
| [20] | 林立铭, 王琴飞, 余厚美, 等. 食用木薯块根冻结特性及代谢产物分析. 食品工业科技, 2022, 43(15):1-8. |
| [21] | 王琪琪. 黑茶中散囊属真菌及其对茶叶品质提升研究. 贵阳:贵州师范大学, 2021. |
| [22] |
李鑫磊, 俞晓敏, 林军. 基于非靶向代谢组学的白茶与绿茶、乌龙茶和红茶代谢产物特征比较. 食品科学, 2020, 41(12):197-203.
doi: 10.7506/spkx1002-6630-20190128-358 |
| [23] | 张琴, 黄世安, 林欣, 等. 基于UPLC-MS/MS的3个李品种果实初生代谢物分析. 食品科学, 2022, 43(16):226-234. |
| [24] | 张舒, 王长远, 冯玉超, 等. 气相色谱―质谱联用代谢组学技术分析不同产地稻米代谢物. 食品科学, 2021, 42(8):206-213. |
| [25] |
Ali R, Bushra S, Ali R, et al. Metabolomics: a way forward for crop improvement. Metabolites, 2019, 9(12):1-2.
doi: 10.3390/metabo9010001 |
| [26] | Seyed M N, Dunja Š, Michał T, et al. Flavonoid biosynthetic pathways in plants: Versatile targets for metabolic engineering. Biotechnology Advances, 2020, 38(13):5-6. |
| [27] | 刘炎. 植物黄酮类化合物功能的研究进展. 科技信息, 2012 (18):131-132. |
| [28] | 胡云霞, 樊金玲, 武涛. 黄酮类化合物分类和生物活性机理. 枣庄学院学报, 2014, 31(2):72-78. |
| [29] |
Rozmer Z, Perjési P. Naturally occurring chalcones and their biological activities. Phytochemistry Reviews, 2016, 15(1):87- 120.
doi: 10.1007/s11101-014-9387-8 |
| [30] | 赵宽, 周葆华, 马万征, 等. 不同环境胁迫对根系分泌有机酸的影响研究进展. 土壤, 2016, 48(2):235-240. |
| [31] | 王兰兰, 宋晓卉, 杨笛, 等. 环境条件对植物有机酸影响研究进展. 沈阳师范大学学报(自然科学版), 2019, 37(3):236-239. |
| [32] |
Fatma K, Joachim K, Dale W H, et al. Exploring the temperature- stress metabolome of arabidopsis. Plant Physiology, 2004, 136 (4):4159-4168.
doi: 10.1104/pp.104.052142 |
| [33] |
郭家鑫, 鲁晓宇, 陶一凡, 等. 棉花在盐碱胁迫下代谢产物及通路的分析. 作物学报, 2022, 48(8):2100-2114.
doi: 10.3724/SP.J.1006.2022.14110 |
| [34] | 杨会议. 钯催化烯烃羰基化合成季碳中心酰胺. 西安: 西北大学, 2021. |
| [35] |
De Luca V, St-Pierre B. The cell and developmental biology of alkaloid biosynthesis. Trends in Plant Science, 2000, 5(4):168- 173.
pmid: 10740298 |
| [36] | 乔小燕, 马春雷, 陈亮. 植物类黄酮生物合成途径及重要基因的调控. 天然产物研究与开发, 2009, 21(2):354-360,207. |
| [37] | 郭凤丹, 王效忠, 刘学英, 等. 植物花青素生物代谢调控. 生命科学, 2011, 23(10):938-944. |
| [38] | 辛宇, 孙敬蒙, 张炜煜. 花青素生物活性及制剂的研究进展. 食品工业科技, 2021, 42(17):413-422. |
| [1] | 高艳梅, 冯鹏睿, 陈薇薇, 张萌, 张永清. 抗旱性藜麦幼苗对干旱胁迫的生理响应[J]. 作物杂志, 2026, (1): 182–188 |
| [2] | 王亮, 王睿, 朱金成, 桑玉伟, 史彪, 郭嘉帅, 焦灰敏, 何宗铃, 水涌. 50份花生品种(系)幼苗期耐盐性分析[J]. 作物杂志, 2025, (5): 35–41 |
| [3] | 张金东, 王成, 卢环, 曾玲玲, 张巩亮, 孙浩月, 刘悦, 杨贺麟, 侯晓敏. 盐碱胁迫下不同基因型绿豆对外源BR的响应[J]. 作物杂志, 2025, (5): 54–60 |
| [4] | 赵洲, 张丽, 高新磊, 邱鸿雨. 复合盐碱胁迫对燕麦生长及代谢的影响[J]. 作物杂志, 2025, (5): 74–85 |
| [5] | 褚霈宇, 韩喜财, 王盼, 李多, 朱浩, 金喜军, 宋鑫玲, 曹洪勋, 夏尊民, 王晓楠. 水分胁迫下CaCl2对亚麻幼苗生长及生理的影响[J]. 作物杂志, 2025, (4): 206–213 |
| [6] | 黄明, 付鑫鑫, 张振旺, 张军, 李友军. 种子大小对旱地小麦种子萌发、幼苗特性和抗旱性的影响[J]. 作物杂志, 2025, (3): 255–262 |
| [7] | 景茂雅, 张子玉, 张萌, 合佳敏, 严翻翻, 高艳梅, 张永清. 水杨酸浸种对盐胁迫藜麦种子萌发及幼苗生长的影响[J]. 作物杂志, 2025, (1): 194–201 |
| [8] | 鄂利锋, 徐金崇, 陈修斌, 权建华, 华军, 尹丽娟, 王舜奇, 赵文勤. 外源硅对盐胁迫下娃娃菜种子萌发及幼苗生理特性的影响[J]. 作物杂志, 2024, (6): 212–217 |
| [9] | 张旭丽, 王瑞军, 郗小倩, 冯学金, 李洪. 干旱胁迫及复水对黄芪幼苗生长、生理特性及次生代谢产物积累的影响[J]. 作物杂志, 2024, (5): 204–211 |
| [10] | 张子怡, 王学虎, 苑莹, 沈志峰. 腐植酸悬浮剂对NaCl胁迫下小麦种子萌发和幼苗生长的影响[J]. 作物杂志, 2024, (4): 263–268 |
| [11] | 卿晨, 刘正学, 李彦杰. 转录组测序分析干旱胁迫下复合微生物菌肥对玉米幼苗抗旱性的影响[J]. 作物杂志, 2024, (3): 32–39 |
| [12] | 李盛, 李翔, 朱美如, 王夏, 李昊阳, 谭欣如, 王海燕. 马铃薯青枯病拮抗菌的筛选及温室防治效果研究[J]. 作物杂志, 2024, (2): 242–248 |
| [13] | 刘佳, 吴天一, 朱嘉宇, 邓绍珠, 张玉先, 梁喜龙, 金喜军. 烯效唑与褪黑素复配对红小豆萌发和根系形态的影响[J]. 作物杂志, 2024, (1): 180–186 |
| [14] | 姜珊, 刘佳, 曹亮, 任春元, 金喜军, 张玉先. 外源褪黑素对干旱胁迫下红小豆幼苗生长和产量的影响[J]. 作物杂志, 2023, (4): 202–209 |
| [15] | 傅晓艺, 王红光, 刘志连, 李东晓, 何明琦, 李瑞奇. 水分胁迫对不同小麦幼苗期生长的影响及抗旱品种筛选[J]. 作物杂志, 2023, (4): 224–229 |
|
||