作物杂志,2021, 第5期: 153–159 doi: 10.16035/j.issn.1001-7283.2021.05.023
甘薯轮作与间作对根际土壤微生物群落的影响
胡启国( ), 刘亚军(
), 刘亚军( ), 王文静, 王祁, 王红刚, 储凤丽
), 王文静, 王祁, 王红刚, 储凤丽
- 商丘市农林科学院,476000,河南商丘
Effects of Sweet Potato Rotation and Intercropping on the Microbial Community of Rhizosphere Soil
Hu Qiguo( ), Liu Yajun(
), Liu Yajun( ), Wang Wenjing, Wang Qi, Wang Honggang, Chu Fengli
), Wang Wenjing, Wang Qi, Wang Honggang, Chu Fengli
- Shangqiu Academy of Agriculture and Forestry Sciences, Shangqiu 476000, Henan, China
摘要:
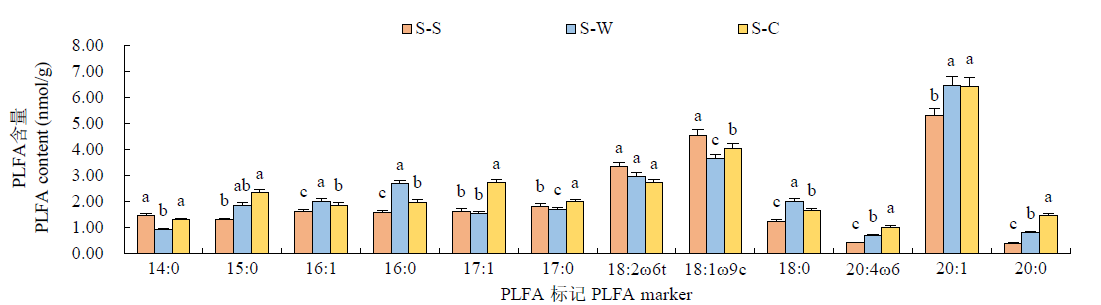
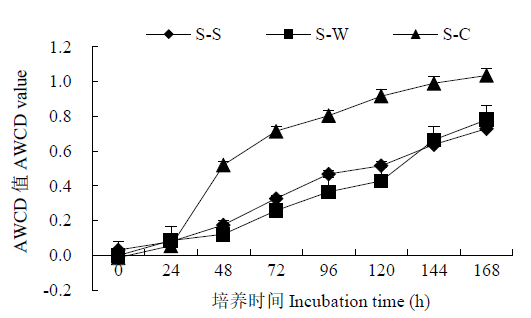
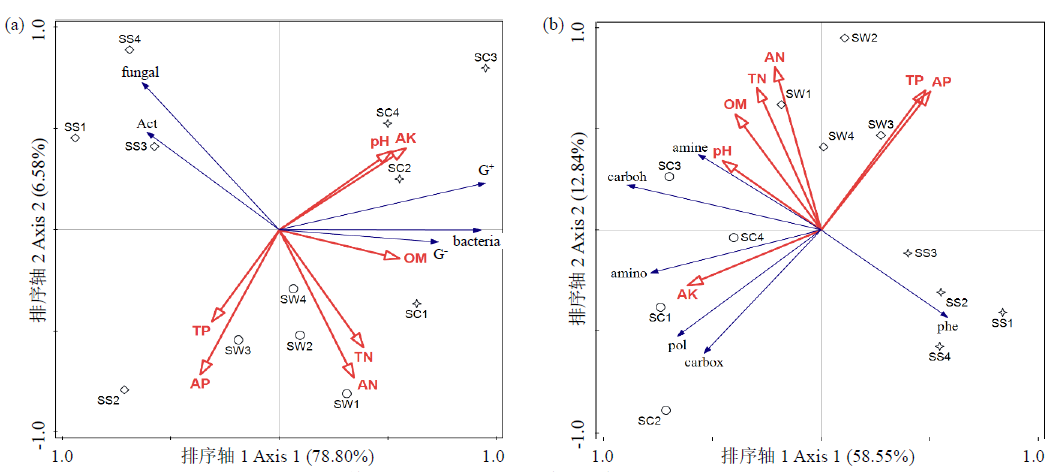
为揭示土壤微生物群落对甘薯不同种植制度的响应机制,通过田间定位试验,设置甘薯连作、甘薯–小麦轮作、甘薯–玉米间作3个处理,采用磷脂脂肪酸(PLFA)和生态板(BIOLOG ECO)技术手段,研究了轮作与间作对甘薯根际土壤微生物群落结构、碳源利用能力的影响。结果表明,与甘薯连作处理相比,轮作与间作改变了土壤微生物主要类别的PLFA生物量,甘薯–小麦轮作与甘薯–玉米间作处理的细菌含量分别显著(P<0.05)增加21.82%和38.77%,放线菌含量分别显著增加6.98%和12.77%,革兰氏阳性菌生物量分别显著增加28.60%和63.44%,革兰氏阴性菌生物量分别显著增加18.21%和22.29%,真菌含量分别显著降低16.60%和13.03%;随着培养时间的延长,甘薯–玉米间作处理的平均颜色变化率(AWCD值)显著高于其他2个处理,甘薯–玉米间作处理对羧酸类化合物、多聚化合物、碳水化合物、氨基酸化合物和胺类化合物的利用能力较甘薯连作处理分别显著增加17.28%、14.67%、54.17%、36.62%和20.00%;冗余分析(RDA)结果表明,土壤微生物群落结构及功能多样性的变化受多种因素共同影响,土壤速效钾和全氮为主要驱动因子;甘薯–小麦轮作与甘薯–玉米间作在一定程度上均可优化土壤微生物群落结构,提升微生物功能多样性,其中甘薯–玉米间作处理效果较好。
| [1] | 刘亚军, 胡启国, 储凤丽, 等. 不同栽培模式对甘薯干物质分配及产量的影响. 黑龙江八一农垦大学学报, 2018, 30(6):1-7,18. |
| [2] | 吴燕, 颜朗, 李雪丹, 等. 甘薯耐旱和耐盐基因的挖掘和表达分析. 四川大学学报(自然科学版), 2016, 53(5):1147-1154. |
| [3] | 高志远, 胡亚亚, 刘兰服, 等. 甘薯连作对根际土壤微生物群落结构的影响. 核农学报, 2019, 33(6):1248-1255. |
| [4] | 马代夫, 李强, 曹清河, 等. 中国甘薯产业及产业技术的发展与展望. 江苏农业学报, 2012, 28(5):969-973. |
| [5] | 张树生, 杨兴明, 茆泽圣, 等. 连作土灭菌对黄瓜(Cucumis sativus)生长和土壤微生物区系的影响. 生态学报, 2007, 27(5):1809-1817. |
| [6] | 李晶晶, 李煊桢, 李振方, 等. 不同种植土壤对地黄生长和酶活性及其根际土壤微生态的影响. 植物资源与环境学报, 2015, 24(1):42-47. |
| [7] | 王灿, 李志刚, 杨建峰, 等. 胡椒连作对土壤微生物群落功能多样性与群落结构的影响. 热带作物学报, 2017, 38(7):1235-1242. |
| [8] |
Kumar A, Padhy S R J, Das R R, et al. Elucidating relationship between nitrous oxide emission and functional soil microbes from tropical lowland rice soil exposed to elevated CO2:A path modelling approach. Agriculture, Ecosystems and Environment, 2021, 308:107268.
doi: 10.1016/j.agee.2020.107268 |
| [9] |
吴林坤, 林向民, 林文雄. 根系分泌物介导下植物-土壤-微生物互作关系研究进展与展望. 植物生态学报, 2014, 38(3):298-310.
doi: 10.3724/SP.J.1258.2014.00027 |
| [10] |
Li C P, Shi W C, Wu D, et al. Biocontrol of potato common scab by Brevibacillus laterosporus BL12 is related to the reduction of pathogen and changes in soil bacterial community. Biological Control, 2021, 153:104496.
doi: 10.1016/j.biocontrol.2020.104496 |
| [11] | 商丽丽, 杜清福, 韩俊杰, 等. 甘薯重茬对土壤微生物的影响及重茬障碍防治措施研究. 作物杂志, 2015(4):126-129. |
| [12] | 谭雪莲. 轮作模式下马铃薯土壤微生物多样性、酶活性及根系分泌物的研究. 兰州:甘肃农业大学, 2016. |
| [13] | 宋佳承. 轮作及连作对马铃薯生长发育及根际微环境的影响. 兰州:甘肃农业大学, 2020. |
| [14] | 金莉. 不同蔬菜轮作对温室番茄连作基质微生物多样性及番茄生长的影响. 兰州:甘肃农业大学, 2020. |
| [15] | 姚小东, 李孝刚, 丁昌峰, 等. 连作和轮作模式下花生土壤微生物群落不同微域分布特征. 土壤学报, 2019, 56(4):975-985. |
| [16] |
Timothy S, Prather W, Thomas L, et al. Interplanting grasses into alfalfa controls weeds in older stands. California Agriculture, 2000, 54(6):37-41.
doi: 10.3733/ca.v054n06p37 |
| [17] | 赵军. 苏南地区稻麦轮作系统的高产土壤微生物区系培育与调控研究. 南京:南京农业大学, 2016. |
| [18] | 孙倩. 轮作模式对谷茬地作物根际土壤特性及微生物群落多样性的影响. 银川:宁夏大学, 2019. |
| [19] | 王劲松, 樊芳芳, 郭珺, 等. 不同作物轮作对连作高粱生长及其根际土壤环境的影响. 应用生态学报, 2016, 27(7):2283-2291. |
| [20] | 刘贤文, 郭华春. 马铃薯与玉米复合种植对土壤化感物质及土壤细菌群落结构的影响. 中国生态农业学报(中英文), 2020, 28(6):794-802. |
| [21] | 严君, 韩晓增, 陈旭, 等. 施肥对小麦、玉米和大豆连作土壤微生物群落功能多样性的影响. 干旱地区农业研究, 2019, 37(6):171-177. |
| [22] | 孙小花, 胡新元, 陆立银, 等. 黄土高原马铃薯不同连作年限土壤理化性质及微生物特性. 干旱地区农业研究, 2019, 37(4):184-192. |
| [23] | 刘亚军. 马铃薯不同间作模式对作物与土壤的影响. 银川:宁夏大学, 2017. |
| [24] |
Massaccesi L, Benucci G M N, Gigliotti G, et al. Rhizosphere effect of three plant species of environment under periglacial conditions (Majella Massif,central Italy). Soil Biology and Biochemistry, 2015, 89:184-195.
doi: 10.1016/j.soilbio.2015.07.010 |
| [25] | 张秋芳, 刘波, 林营志, 等. 土壤微生物群落磷脂脂肪酸PLFA生物标记多样性. 生态学报, 2009, 29(8):4127-4137. |
| [26] |
Campbell C D, Grayston S J, Hirst D J. Use of rhizosphere carbon sources in sole carbon source tests to discriminate soil microbial communities. Journal of Microbiological Methods, 1997, 30(1):33-41.
doi: 10.1016/S0167-7012(97)00041-9 |
| [27] | 王光州. 土壤微生物调节植物种间互作和多样性―生产力关系的机制. 北京:中国农业大学, 2018. |
| [28] | 徐海强, 黄洁, 刘子凡, 等. 木薯/花生间作对其根际土壤微生物数量、群落结构及多样性的影响. 南方农业学报, 2016, 47(2):185-190. |
| [29] |
Hao W Y, Ren L X, Ran W, et al. Allelopathic effects of root exudates from watermelon and rice plants on Fusarium oxysporum f. sp. niveum. Plant and Soil, 2010, 336:485-497.
doi: 10.1007/s11104-010-0505-0 |
| [30] | Li P, Ma L, Feng Y L, et al. Diversity and chemotaxis of soil bacteria with antifungal activity against Fusarium wilt of banana. Journal of Industrial Microbiology, 2012, 39:1495-1505. |
| [31] | 黄玉茜, 韩晓日, 杨劲峰, 等. 花生根系分泌物对土壤微生物学特性及群落功能多样性的影响. 沈阳农业大学学报, 2015, 46(1):48-54. |
| [32] | 杨智仙, 汤利, 郑毅, 等. 不同品种小麦与蚕豆间作对蚕豆枯萎病发生、根系分泌物和根际微生物群落功能多样性的影响. 植物营养与肥料学报, 2014, 20(3):570-579. |
| [33] | 董宇飞, 吕相漳, 张自坤, 等. 不同栽培模式对辣椒根际连作土壤微生物区系和酶活性的影响. 浙江农业学报, 2019, 31(9):1485-1492. |
| [34] | 唐艳芬, 续勇波, 郑毅, 等. 小麦蚕豆间作对根际土壤氮转化微生物的影响. 农业资源与环境学报, 2016, 33(5):482-490. |
| [35] |
Gao Z, Han M, Hu Y, et al. Effects of continuous cropping of sweet potato on the fungal community structure in rhizospheric soil. Frontiers in Microbiology, 2019, 10:2269.
doi: 10.3389/fmicb.2019.02269 |
| [36] |
Bais H P, Weir T L, Perry L G, et al. The role of root exudates in rhizosphere interactions with plants and other organisms. Annual Review of Plant Biology, 2006, 57:233-266.
doi: 10.1146/arplant.2006.57.issue-1 |
| [37] | 刘亚军, 马琨, 李越, 等. 马铃薯间作栽培对土壤微生物群落结构与功能的影响. 核农学报, 2018, 32(6):1186-1194. |
| [38] | 许建晶. 陇中黄土高原坡耕地土壤碳组分和微生物功能多样性对间作体系的响应. 兰州:甘肃农业大学, 2018. |
| [1] | 吴鑫雨, 刘振洋, 李海叶, 郑毅, 汤利, 肖靖秀. 施氮和间作对蚕豆根瘤形成及氮素吸收累积的影响[J]. 作物杂志, 2021, (5): 120–127 |
| [2] | 唐红琴, 李忠义, 董文斌, 韦彩会, 何铁光, 蒙炎成, 汤海玲, 莫永诚. 不同间作绿肥替代化肥模式对木薯性状和产量的影响[J]. 作物杂志, 2021, (4): 184–190 |
| [3] | 范业赓, 陈荣发, 闫海锋, 周慧文, 翁梦苓, 黄杏, 罗霆, 周忠凤, 丘立杭, 吴建明. 甘蔗轮作青饲玉米和花生对甘蔗生长和土壤性状的影响[J]. 作物杂志, 2021, (1): 104–111 |
| [4] | 刘佳敏, 汪洋, 褚旭, 齐欣, 王慢慢, 赵亚南, 叶优良, 黄玉芳. 种植密度和施氮量对小麦-玉米轮作体系下周年产量及氮肥利用率的影响[J]. 作物杂志, 2021, (1): 143–149 |
| [5] | 谢金兰, 林丽, 李长宁, 罗霆, 莫璋红. 氮肥减量条件下间作绿豆压青对甘蔗生长及氮代谢的影响[J]. 作物杂志, 2020, (4): 164–169 |
| [6] | 宋秋来, 王麒, 冯延江, 孙羽, 曾宪楠, 来永才. 寒地水旱轮作及秸秆还田对土壤相关酶活性的影响[J]. 作物杂志, 2020, (3): 149–153 |
| [7] | 郭琪琳,吴海云,李欢,刘庆. 不同类型甘薯茎和叶中碳、氮、磷化学计量学特征研究[J]. 作物杂志, 2020, (2): 41–47 |
| [8] | 孟凡来,郭华春. UV-B辐射增强对甘薯光合特性和紫外吸收物质的影响[J]. 作物杂志, 2019, (5): 114–119 |
| [9] | 张海斌,蒙美莲,刘坤雨,章凌翔,陈有君. 不同轮作模式对马铃薯干物质积累、病害发生及产量的影响[J]. 作物杂志, 2019, (4): 170–175 |
| [10] | 权宝全,吕瑞洲,王贵江,任杰成. 薯块膨大中期不同栽培措施对甘薯生长发育及产量的影响[J]. 作物杂志, 2019, (3): 158–161 |
| [11] | 代希茜,詹和明,崔兴洪,赵银月,单丹丹,张亮,王铁军. 玉米大豆间作种植密度耦合数学模型及其优化方案研究[J]. 作物杂志, 2019, (2): 128–135 |
| [12] | 刘亚军,储凤丽,王文静,胡启国,杨爱梅. 不同配套栽培措施对商薯9号产量及杂草防控的影响[J]. 作物杂志, 2019, (2): 179–184 |
| [13] | 白雨,韩雪莹,董海洋,乌云苏都,李冰圳,陈贵林. 轮作及农艺措施对减轻向日葵列当危害的影响[J]. 作物杂志, 2019, (2): 192–196 |
| [14] | 柏文恋,郑毅,肖靖秀. 豆科禾本科间作促进磷高效吸收利用的地下部生物学机制研究进展[J]. 作物杂志, 2018, (4): 20–27 |
| [15] | 刘亚军,胡启国,储凤丽,王文静,杨爱梅. 不同栽培方式和种植密度对“商薯9号”产量及结薯习性的影响[J]. 作物杂志, 2018, (4): 89–94 |
|
||